Questões de Vestibular
Sobre propriedades coligativas: tonoscopia, ebulioscopia, crioscopia e pressão osmótica. em química
Foram encontradas 90 questões
A importância da água. Toda Matéria. Disponível em:<https://www.todamateria.com.br/a-importancia-da-agua/>. Acesso em: 07 set. 2017. Adaptado.
A respeito da substância água, marque a alternativa INCORRETA.

Pesquisadores da Universidade da Califórnia, Estados Unidos, e do Instituto Central de Pesquisa do Sal e Química, em Gujarat, Índia, estão trabalhando com outros estudiosos da Universidade de Ben-Gurion do Negev, Israel, no cultivo de plantas modificadas geneticamente, MGs, como o arroz Oryza sativa, cevada e tomate em água de baixa qualidade, salobra a reciclada e até água marinha diluída — a concentração média de cloreto de sódio, NaCl, na água do mar é de 30gL−1 . O objetivo do estudo é desenvolver cultivares, MGs, com genes de holófitas a sobreviverem na presença de sal e alimentarem bilhões de pessoas até os meados do século. Quase 25% das áreas irrigadas do mundo sofrem com os solos salinizados arruinados devido à prática de irrigação inadequada. Cientistas estão tentando adicionar as proteínas transportadoras de ions Na+ (aq) e Cl− (aq) nas antiportes das halófitas e plantas, como o arroz, que produz mais de 40% de grãos na presença da água marinha, com um décimo de concentração de sal.
FIGURA 05

Com relação a esse experimento, o aluno pode ter observado:
I - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a temperatura de ebulição da solução seja superior à do solvente.
II - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a temperatura de fusão da solução seja inferior à do solvente.
III - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a pressão máxima de vapor da solução seja inferior à do solvente quando ambas são submetidas à mesma temperatura.
IV- A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a pressão osmótica da solução seja superior à do solvente.
Considere as três soluções aquosas abaixo:
(1) Al(NO3)3 0,10 mol/L (2) FeCl2 0,133 mol/L (3) Na2SO4 0,300 mol/L
Assinale a alternativa que representa as informações corretas acerca das temperaturas de ebulição das soluções.
Sobre esse tema, correlacione as colunas A e B.
Coluna A (1) Ebulioscopia (2) Osmometria (3) Crioscopia
Coluna B ( ) Ao se adicionar etilenoglicol à água dos radiadores dos carros, evita-se o congelamento, em países que nevam. ( ) Ao se adicionar sal de cozinha (NaCl) à água fervente, observa-se o cessar da fervura. ( ) Ao colocar ameixas secas em água, com o tempo, nota-se que as ameixas incham.
Assinale a alternativa que contém a sequência correta, de cima para baixo.
DADOS QUE PODEM SER USADOS NESTA PROVA:

Assinale a alternativa CORRETA:
Considere as três soluções aquosas a seguir:
Solução A = NaCl 0,1 mol/L Solução B = sacarose 0,1 mol/L Solução C = CaCl2 0,1 mol/L
As soluções foram colocadas em ordem crescente de temperatura de ebulição em
INSTRUÇÃO: Para responder à questão, analise o texto e as afirmativas que seguem.
Uma forma de gelar bebidas rapidamente consiste em preparar um recipiente com gelo e água e adicionar sal grosso ou álcool. A mistura assim produzida é denominada mistura refrigerante, pois atinge temperaturas abaixo de 0 ºC e proporciona um excelente meio de gelar as latas e garrafas colocadas dentro dele.
Sobre esse processo, afirma-se:
I. Uma mistura de gelo, água e açúcar pode ser usada como mistura refrigerante.
II. A temperatura de congelamento de uma mistura de gelo, água e areia é de cerca de 0 ºC.
III. Uma mistura de gelo, água e álcool tem duas fases e três componentes.
IV. A adição de sal grosso ao gelo com água proporciona temperaturas mais baixas do que a adição de sal fino na mesma quantidade.
De acordo com as informações acima, são corretas
apenas as afirmativas

A partir da polimerização de determinado monômero,
realizada em solução com duas diferentes condições reacionais,
chegou-se a polímeros com diferentes distribuições de
massas molares, conforme ilustrado na figura acima. Ao final
dos procedimentos de síntese, as duas soluções obtidas —
uma contendo o polímero A (solução I) e outra, o polímero B
(solução II) — tinham concentrações iguais, em g/L.
Com base nessa situação e considerando que os comportamentos das soluções sejam ideais e que os polímeros sejam estáveis na temperatura de ebulição do solvente empregado em suas sínteses, julgue o item e faça o que se pede no item, que é do tipo C.
A respeito das soluções preparadas, assinale a opção correta.
A solução I apresenta pressão osmótica superior à da
solução II.
Os compostos iônicos e moleculares interferem de formas diferentes na variação da pressão osmótica de um organismo. Como regra geral, podemos afirmar que, considerando uma mesma quantidade de matéria, os efeitos causados pelo consumo de sal são mais intensos que os de açúcar. Considere que soluções aquosas diferentes tenham sido preparadas com 50 g de nitrato de cálcio e 50 g de glicerina (propan-1,2,3-triol), formando dois sistemas em que cada um apresente 2,0 litros de solução a 20 ºC. A razão existente entre a pressão osmótica do sistema salino em relação à pressão osmótica do sistema alcólico é, aproximadamente:
Use 0,082 atm.L/mol.K para a constante universal dos gases perfeitos.
TEXTO 2
VI
Para entenderes bem o que é a morte e a vida, basta contar-te como morreu minha avó.
— Como foi?
— Senta-te.
Rubião obedeceu, dando ao rosto o maior interesse possível, enquanto Quincas Borba continuava a andar.
— Foi no Rio de Janeiro, começou ele, defronte da Capela Imperial, que era então Real, em dia de grande festa; minha avó saiu, atravessou o adro, para ir ter à cadeirinha, que a esperava no Largo do Paço. Gente como formiga. O povo queria ver entrar as grandes senhoras nas suas ricas traquitanas. No momento em que minha avó saía do adro para ir à cadeirinha, um pouco distante, aconteceu espantar-se uma das bestas de uma sege; a besta disparou, a outra imitou-a, confusão, tumulto, minha avó caiu, e tanto as mulas como a sege passaram-lhe por cima. Foi levada em braços para uma botica da Rua Direita, veio um sangrador, mas era tarde; tinha a cabeça rachada, uma perna e o ombro partidos, era toda sangue; expirou minutos depois.
— Foi realmente uma desgraça, disse Rubião.
— Não.
— Não?
— Ouve o resto. Aqui está como se tinha passado o caso. O dono da sege estava no adro, e tinha fome, muita fome, porque era tarde, e almoçara cedo e pouco. Dali pôde fazer sinal ao cocheiro; este fustigou as mulas para ir buscar o patrão. A sege no meio do caminho achou um obstáculo e derribou-o; esse obstáculo era minha avó. O primeiro ato dessa série de atos foi um movimento de conservação: Humanitas tinha fome. Se em vez de minha avó, fosse um rato ou um cão, é certo que minha avó não morreria, mas o fato era o mesmo; Humanitas precisa comer. Se em vez de um rato ou de um cão, fosse um poeta, Byron ou Gonçalves Dias diferia o caso no sentido de dar matéria a muitos necrológios; mas o fundo subsistia. O universo ainda não parou por lhe faltarem alguns poemas mortos em flor na cabeça de um varão ilustre ou obscuro; mas Humanitas (e isto importa, antes de tudo) Humanitas precisa comer.
Rubião escutava, com a alma nos olhos, sinceramente desejoso de entender; mas não dava pela necessidade a que o amigo atribuía a morte da avó. Seguramente o dono da sege, por muito tarde que chegasse à casa, não morria de fome, ao passo que a boa senhora morreu de verdade, e para sempre. Explicou-lhe, como pôde, essas dúvidas, e acabou perguntando-lhe:
— E que Humanitas é esse?
— Humanitas é o princípio. Mas não, não digo nada, tu não és capaz de entender isto, meu caro Rubião; falemos de outra coisa.
— Diga sempre.
Quincas Borba, que não deixara de andar, parou alguns instantes.
— Queres ser meu discípulo?
— Quero.
— Bem, irás entendendo aos poucos a minha filosofia; no dia em que a houveres penetrado inteiramente, ah! nesse dia terás o maior prazer da vida, porque não há vinho que embriague como a verdade. Crê-me, o Humanitismo é o remate das coisas; e eu, que o formulei, sou o maior homem do mundo. Olha, vês como o meu bom Quincas Borba está olhando para mim? Não é ele, é Humanitas...
— Mas que Humanitas é esse?
— Humanitas é o principio. Há nas coisas todas certa substância recôndita e idêntica, um princípio único, universal, eterno, comum, indivisível e indestrutível, — ou, para usar a linguagem do grande Camões:
Uma verdade que nas coisas anda,
Que mora no visíbil e invisíbil.
Pois essa sustância ou verdade, esse princípio indestrutível é que é Humanitas. Assim lhe chamo, porque resume o universo, e o universo é o homem. Vais entendendo?
— Pouco; mas, ainda assim, como é que a morte de sua avó...
— Não há morte. O encontro de duas expansões, ou a expansão de duas formas, pode determinar a supressão de uma delas; mas, rigorosamente, não há morte, há vida, porque a supressão de uma é a condição da sobrevivência da outra, e a destruição não atinge o princípio universal e comum. Daí o carácter conservador e benéfico da guerra. Supõe tu um campo de batatas e duas tribos famintas. As batatas apenas chegam para alimentar uma das tribos, que assim adquire forças para transpor a montanha e ir à outra vertente, onde há batatas em abundância; mas, se as duas tribos dividirem em paz as batatas do campo, não chegam a nutrir-se suficientemente e morrem de inanição. A paz, nesse caso, é a destruição; a guerra é a conservação. Uma das tribos extermina a outra e recolhe os despojos. Daí a alegria da vitória, os hinos, aclamações, recompensas públicas e todos os demais efeitos das ações bélicas. Se a guerra não fosse isso, tais demonstrações não chegariam a dar-se, pelo motivo real de que o homem só comemora e ama o que lhe é aprazível ou vantajoso, e pelo motivo racional de que nenhuma pessoa canoniza uma ação que virtualmente a destrói. Ao vencido, ódio ou compaixão; ao vencedor, as batatas.
— Mas a opinião do exterminado?
— Não há exterminado. Desaparece o fenômeno; a substância é a mesma. Nunca viste ferver água? Hás de lembrar-te que as bolhas fazem-se e desfazem-se de contínuo, e tudo fica na mesma água. Os indivíduos são essas bolhas transitórias.
— Bem; a opinião da bolha...
— Bolha não tem opinião. Aparentemente, há nada mais contristador que uma dessas terríveis pestes que devastam um ponto do globo? E, todavia, esse suposto mal é um benefício, não só porque elimina os organismos fracos, incapazes de resistência, como porque dá lugar à observação, à descoberta da droga curativa. A higiene é filha de podridões seculares; devemo-la a milhões de corrompidos e infectos. Nada se perde, tudo é ganho. Repito, as bolhas ficam na água. Vês este livro? É Dom Quixote. Se eu destruir o meu exemplar, não elimino a obra, que continua eterna nos exemplares subsistentes e nas edições posteriores. Eterna e bela, belamente eterna, como este mundo divino e supradivino.
(ASSIS, Machado de. Quincas Borba. 18. ed. São
Paulo: Ática, 2011. p. 26-28.)
Considere o fragmento do Texto 2: “— Não há exterminado. Desaparece o fenômeno; a substância é a mesma. Nunca viste ferver água? Hás de lembrar-te que as bolhas fazem-se e desfazem-se de contínuo, e tudo fica na mesma água. Os indivíduos são essas bolhas transitórias.”
Ao se colocar uma panela com água mineral para aquecer em um fogão em Goiânia, observa-se que, mesmo que a temperatura esteja abaixo do ponto de evaporação, há a formação de bolhas. Somente com a temperatura próxima de 98°C é que há a evolução muito violenta de bolhas.
A respeito dessa constatação, analise as afirmativas a seguir:
I-A pressão de vapor diminui com a altitude.
II-Crioscopia é a passagem de água do meio menos concentrado para o meio mais concentrado.
III-Ebulioscopia é o estudo do abaixamento da temperatura de ebulição da solução devido à presença de um soluto.
IV-A formação de bolhas na etapa inicial do aquecimento também tem a ver com os gases dissolvidos na água.
Em relação às proposições analisadas, assinale a
única alternativa cujos itens estão todos corretos:
A comparação entre as proporções isotópicas de amostras de um mesmo material, que têm a mesma idade, encontradas em diferentes regiões, pode ser utilizada para revelar se elas têm ou não a mesma origem. Se as proporções são iguais, então é possível que tenham a mesma origem, mas se forem diferentes, é certeza que não têm a mesma origem. A tabela a seguir apresenta os dados de algumas amostras de água, incluindo a de um cometa no qual uma sonda pousou recentemente.
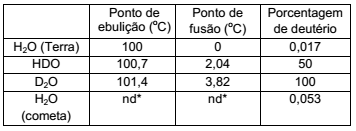
*nd – não disponível
Com base nesses dados, pode-se afirmar corretamente que
a água de nosso planeta
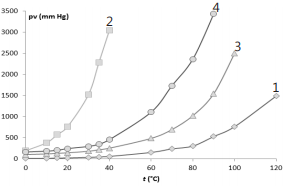
Temperatura (°C) Pressão máxima de vapor de água
no ar atmosférico (mm Hg)
10 9,2
20 17,5
30 31,8
40 55,3
A umidade relativa (UR) é um termo utilizado com frequência pelos meteorologistas para indicar a quantidade de vapor de água presente no ar atmosférico. Em uma mesma temperatura, a UR pode ser obtida pela razão entre a pressão parcial de vapor de água presente no ar e a pressão máxima de vapor de água. Assim, um local onde a temperatura encontra-se a 20 °C e a pressão parcial de vapor de água é igual a 10,5 mm Hg, terá uma UR, em termos percentuais, de
Solução Temperatura de ebulição (ºC)
A 104,2
B 106,7
I. A pressão de vapor de ambas as soluções é menor do que a pressão de vapor da água pura. II. A solução A apresenta menor concentração de sal em relação à concentração salina da solução B. III. As forças de interação intermoleculares na solução B apresentam maior intensidade do que as forças de interação existentes, tanto na solução A como na água.
É correto dizer que
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
Uma solução de cloreto de cálcio utilizada para fins industriais apresenta molalidade 2 e tem ponto de ebulição 103,016 ºC sob pressão de 1 atm. Sabendo que a constante ebulioscópica da água é 0,52 ºC, o seu grau de dissociação iônica aparente é