Questões de Vestibular de Química
Foram encontradas 1.430 questões
A molécula representada a seguir corresponde à forma mais ativa da vitamina E.
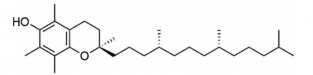
Estão presentes as duas seguintes funções
orgânicas oxigenadas nessa molécula:
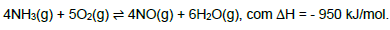
Quando a reação atinge o equilíbrio, uma maneira de aumentar a produção de NO(g) é aumentando a(o):
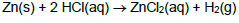
Se 10,00 g de Zn foram misturados com 8,00 g de ácido clorídrico, quantos mols de H2 foram liberados aproximadamente:
I. manter a água em repouso por um tempo adequado, para a deposição, no fundo do recipiente, do material em suspensão mecânica. II. remoção das partículas menores, em suspensão, não separáveis pelo processo descrito na etapa I. III. evaporação e condensação da água, para diminuição da concentração de sais (no caso de água salobra ou do mar). Neste caso, pode ser necessária a adição de quantidade conveniente de sais minerais após o processo.
As etapas I, II e III correspondem, respectivamente, aos processos de separação denominados
Sobre esse assunto, avalie as afirmações seguir
I. A construção de hidrelétricas relaciona-se, também, à preocupação com a crise energética mundial prevista para as próximas décadas. II. As usinas térmicas a gás natural geram tanto monóxido de carbono quanto as usinas movidas a petróleo ou a carvão mineral. III. No processo de geração de energia limpa de origem vegetal emite-se menor quantidade de poluentes atmosféricos do que no processo de fontes de origem fóssil.
É correto o que se afirma em
Considere as afirmações e a reação abaixo.
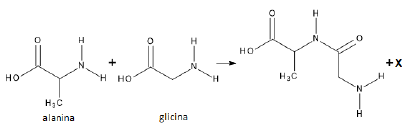
I – Alanina e glicina são aminoácidos.
II – Na reação, forma-se uma ligação peptídica.
III – X indica uma molécula de H2O.
Assinale a alternativa correta.
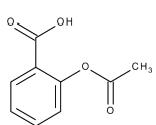
Dados: C = 12,0; H = 1,0; O = 16,0 g/mol. A concentração, em mol/L, de AAS na solução é
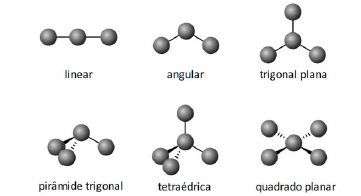
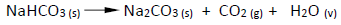
A termólise de 84 g do reagente produzirá a massa de carbonato de sódio e o número de mols de dióxido de carbono iguais a, respectivamente,
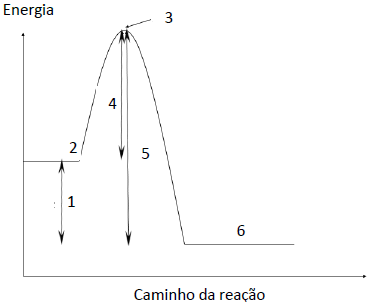
Energia de ativação, variação de entalpia da transformação e complexo ativado podem ser, respectivamente, associados aos números
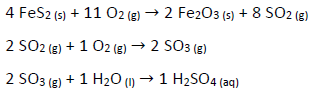
Considere as afirmações: I. O pentóxido de vanádio é um catalisador heterogêneo no meio reacional. II. Os altos valores de temperatura e pressão levam ao aumento das colisões efetivas, o que diminui a energia de ativação. III. A formação de dióxido de enxofre consiste em uma reação de oxirredução, em que o oxigênio sofre oxidação, e o enxofre, redução.
Está correto o que se afirma em