Questões de Vestibular Comentadas sobre química
Foram encontradas 1.427 questões
Temperatura (°C) Kw pH 0 1,14 × 10–15 7,47 10 2,95 × 10–15 7,27 20 1,00 × 10–14 7,00 30 1,47 × 10–14 6,83 50 5,30 × 10–14 6,27
Analisando-se os dados, pode-se afirmar, corretamente, que a
Co+2 + 2e- → Co(s) Eº = - 0.28 V
4e- + O2 (g) + 4 H+ → 2H2O Eº = 1.23V
Após a passagem, pela célula, de uma corrente de 5.0 A durante 1.5 h, as massas de cobalto metálico e de gás oxigênio produzidas são, respectivamente:
Sabe-se pKa = - logKa = 7.20, em que Ka é a constante de dissociação do H2 PO4 - em água a 25 ºC.
O pH da primeira solução e a relação do pH da segunda solução com o pH da primeira são, respectivamente:
A capsantina é um corante vermelho natural da classe das xantofilas . Ela é o principal carotenoide no pimentão vermelho ( Capsicum annuum ) e um componente da oleorresina de pimentão .
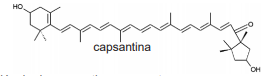
A molécula de capsantina apresenta
(i) Uma amostra de massa 0.3 g foi dissolvida em água e titulada com solução padrão de HCl 0.1 M.
(ii) Até que o ponto final da titulação fosse marcado pela fenolftaleína, foram consumidos 9.0 mL do volume do titulante (HCl).
(iii) O indicador metilorange foi adicionado. Com as duas titulações, até o ponto final marcado pela mudança de cor do indicador metilorange, foram consumidos 30 mL do volume do titulante.
Respectivamente, os percentuais de carbonato e de bicarbonato na amostra original são de:
Considerando-se desprezível o volume do tubo de comunicação e sabendo-se que o volume do balão A é igual a 4.1 L e que a temperatura foi mantida em 27 ºC durante todo processo, o volume do balão B corresponde a:
Um dos mais importantes processos industriais é a fixação do nitrogênio através de sua transformação em amônia, podendo ser representado pela equação a seguir:
N2
(g) + 3H2
(g)  2NH3(g) ΔH = - 92kJ.mol-1
2NH3(g) ΔH = - 92kJ.mol-1
Em relação a esse processo, haverá maior concentração do produto quando ocorrer
Cada estudante recebeu um recipiente contendo 800 mL de água destilada com algumas gotas do indicador de pH alaranjado de metila e soluções de HCl e NaOH em diversas concentrações.
Cada estudante deveria jogar apenas uma vez dois dados, um amarelo e um vermelho, ambos contendo os números de 1 a 6.
• Ao jogar o dado vermelho, o estudante deveria adicionar ao recipiente 100 mL de solução do ácido clorídrico na concentração 10−n mol/L,sendo n o número marcado no dado (por exemplo, se saísse o número 1 no dado, a solução seria de 10−1 mol/L; se saísse 6, a solução seria de 10−6 mol/L). • Ao jogar o dado amarelo, o estudante deveria executar o mesmo procedimento, mas substituindo o ácido por NaOH, totalizando assim 1,0 L de solução. • O estudante deveria observar a cor da solução ao final do experimento.
A professora mostrou a tabela com alguns valores de pH resultantes conforme os números tirados nos dados. Ela pediu, então, aos estudantes que utilizassem seus conhecimentos e a tabela para prever em quais combinações de dados a cor final do indicador seria vermelha.
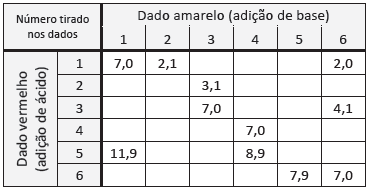
A probabilidade de, após realizar o procedimento descrito, a solução final preparada por um estudante ser vermelha é de:
Note e adote:
Considere a seguinte relação entre pH do meio e coloração do indicador alaranjado de metila:
Menor que 3,3 3,3 a 4,4 Maior que 4,4 Vermelho Laranja Amarelo
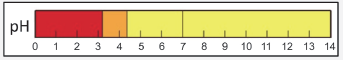
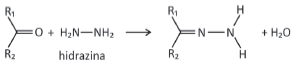
pode ser explorada para a quantificação de compostos cetônicos gerados, por exemplo, pela respiração humana. Para tanto, uma hidrazina específica, a 2,4‐dinitrofenilhidrazina, é utilizada como reagente, gerando um produto que possui cor intensa.
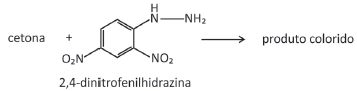
Considere que a 2,4‐dinitrofenilhidrazina seja utilizada para quantificar o seguinte composto:
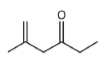
Nesse caso, a estrutura do composto colorido formado será:
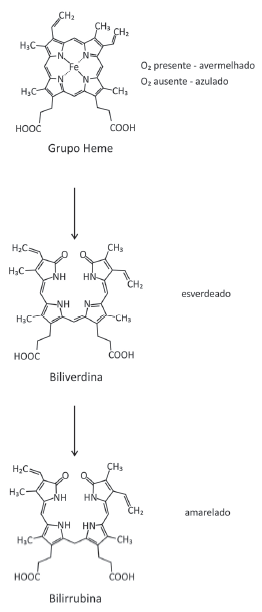
Com base nas informações e nas representações, é correto afirmar:
Considerando um referencial no qual as moléculas neutras encontram‐se paradas antes e após a colisão, a alternativa que melhor representa o arranjo de íons e moléculas instantes antes e instantes depois de uma colisão que leva à reação F − + H3CCl → CH3F + Cl −
é
Note e adote:
Massas atômicas: H = 1 u.m.a., C = 12 u.m.a., F = 19 u.m.a. e Cl = 35 u.m.a. Considere que apenas o isótopo de cloro Cl = 35 u.m.a. participa da reação.
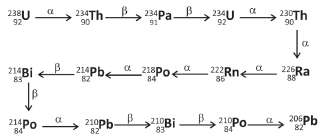
Com base nessas informações e em seus conhecimentos, é correto afirmar:
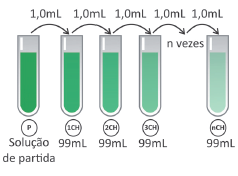
Alguns desses produtos homeopáticos são produzidos com até 200 diluições centesimais sequenciais (200CH).
Considerando uma solução de partida de 100 mL com concentração 1 mol/L de princípio ativo, a partir de qual diluição centesimal a solução passa a não ter, em média, nem mesmo uma molécula do princípio ativo?
Note e adote:
Número de Avogadro = 6×1023.

Note e adote:
Massas molares (g/mol): Licopeno = 537; betanina = 551.


Note e adote:
Temperatura de fusão da sacarose à pressão ambiente = 186 °C; Solubilidade da sacarose a 20 °C = 1,97 kg/L de água.
Considere as quatro reações químicas em equilíbrio apresentadas abaixo.
I H2 (g) + I2 (g) ⇋ 2 HI (g)
II 2 SO2 (g) + O2 (g) ⇋ 2 SO3 (g)
III CO (g) + NO2 (g) ⇋ CO2 (g) + NO (g)
IV 2 H2O (g) ⇋ 2 H2(g) + O2 (g)
Após submetê-las a um aumento de pressão, o deslocamento do equilíbrio gerou aumento
também na concentração dos produtos na seguinte reação:
Para a análise do teor de ozônio em um meio aquoso, utiliza-se iodeto de potássio e ácido sulfúrico. Esses compostos reagem conforme a seguinte equação:
x KI + O3 + H2 SO4 → y I2 + H2O + K2SO4