Questões de Vestibular Comentadas sobre química
Foram encontradas 1.405 questões
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Quando o presidente da Embrapii diz que a glicose é
metade da molécula de sacarose, ele se refere ao fato de
que a molécula de sacarose é formada por duas moléculas
de glicose.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Na presença de hidróxido de sódio, o ácido cítrico reage
produzindo um sabão.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Em solução aquosa, o ácido cítrico sofre três reações de dissociação ácida, cujas equações químicas estão corretamente expressas a seguir.
C6H8O7(aq) + H2O(l) ⇌ C6H7O7 − (aq) + H3O+ (aq)
C6H7O7 − (aq) + H2O(l) ⇌ C6H6O7 2−(aq) + H3O+ (aq)
C6H6O7
2−(aq) + H2O(l) ⇌ C6H5O7
3−(aq) + H3O+
(aq)
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
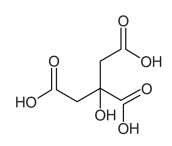
A seguir, é apresentada a fórmula estrutural correta do ácido
cítrico.
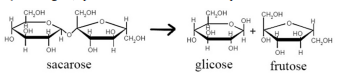
A conversão de sacarose em glicose ocorre por meio da reação a seguir, que tem frutose como outro produto.
Tendo como referência a reação precedente, julgue o item a seguir.
A glicose é a unidade básica de várias moléculas de
importância energética, como o amido e o glicogênio, sendo
este último armazenado no fígado e nos miócitos.
A conversão de sacarose em glicose ocorre por meio da reação a seguir, que tem frutose como outro produto.

Tendo como referência a reação precedente, julgue o item a seguir.
Se NaOH for acrescentado a uma solução aquosa de glicose,
será formado um sal de ácido carboxílico.
A conversão de sacarose em glicose ocorre por meio da reação a seguir, que tem frutose como outro produto.

Tendo como referência a reação precedente, julgue o item a seguir.
A massa molecular da sacarose é igual à massa molecular da
glicose somada à massa molecular da frutose.
A conversão de sacarose em glicose ocorre por meio da reação a seguir, que tem frutose como outro produto.

Tendo como referência a reação precedente, julgue o item a seguir.
A sacarose é um dissacarídeo formado pelos
monossacarídeos glicose e galactose e é digerida no
estômago pela ação da tripsina.
A conversão de sacarose em glicose ocorre por meio da reação a seguir, que tem frutose como outro produto.

Tendo como referência a reação precedente, julgue o item a seguir.
As moléculas de glicose e frutose mostradas na reação são
isômeras de função.
Com relação ao etanol, um dos principais produtos obtidos a partir da cana-de-açúcar, julgue o item que se segue.
O etanol é um biocombustível não renovável e menos
poluente em comparação à gasolina, que é um combustível
fóssil.
Com relação ao etanol, um dos principais produtos obtidos a partir da cana-de-açúcar, julgue o item que se segue.
Na produção do etanol por fermentação alcoólica, ocorre
liberação de CO2.
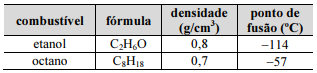
Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue os item.
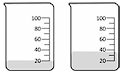
Considerando a combustão total, assinale a opção que representa corretamente os volumes dos combustíveis octano (à esquerda) e etanol (à direita) que devem ser queimados para que haja emissão de uma quantidade equivalente de CO2 pelos dois compostos.

Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item.
No etanol, os comprimentos das ligações entre os átomos de
hidrogênio e os átomos vizinhos são equivalentes entre si.

Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item.
Considere que um íon dicromato (Cr2O7 2- ), de coloração alaranjada, tenha reagido em meio ácido para formar o íon cromo (III), de coloração verde, conforme semirreação a seguir.
Cr2O7 2− + 14 H+ + 6 e− → 2 Cr3+ 7 H2O
Considere, ainda, que, após gotejar excesso de uma solução
ácida de dicromato em dois tubos de ensaio, um contendo
octano e outro etanol, um dos tubos tenha formado uma
solução verde. Dessas informações conclui-se que o tubo de
ensaio cuja solução ficou verde continha etanol e que um dos
produtos formados foi o ácido etanoico.

Maior causador do efeito estufa, o CO2 é liberado pela queima de combustíveis como o octano, um dos principais componentes da gasolina, e o etanol, obtido de biomassa. A esse respeito e considerando os dados na tabela precedente, julgue o item.
Considere-se que a densidade da água seja 1,0 g/cm3 e que o seu ponto de fusão seja 0 ºC. Nesse caso, é correto afirmar que, em uma mistura que contém partes iguais de octano, etanol e água, a 25 ºC, os seus componentes, após o equilíbrio, se posicionarão como apresentado na figura a seguir.
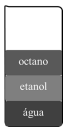
Tendo como referência as informações precedentes, julgue o item que se segue.
O ânion do composto da siderita tem geometria molecular
tetraédrica.
Tendo como referência as informações precedentes, julgue o item que se segue.
O valor da variação de entalpia molar da reação em relação
à hematita, que reage com o monóxido de carbono,
produzindo apenas ferro metálico e dióxido de carbono, é
3 ΔHI + 2 ΔHII +ΔHIII.
Tem-se como exemplo do colonialismo e biopirataria no Brasil o caso do cupuaçu, fruto amazônico de sabor doce e polpa grossa, que serve como fonte de alimento tanto para as populações indígenas quanto para os animais que vivem na região. O cupuaçu é rico em substâncias importantes para a saúde, como fósforo e vitaminas B1 (tiamina), B2 (riboflavina) e B5 (ácido pantotênico). Após uma empresa estrangeira registrar o nome cupuaçu como a Cupuacu International Inc., todos os produtores brasileiros eram obrigados a pagar royalties a essa empresa, sempre que exportassem produtos à base do fruto amazônico. Graças à repercussão desse caso, as ONGs, junto à opinião pública, conseguiram pressionar o escritório de patentes estrangeiro para cancelar o registro da marca “cupuaçu”.
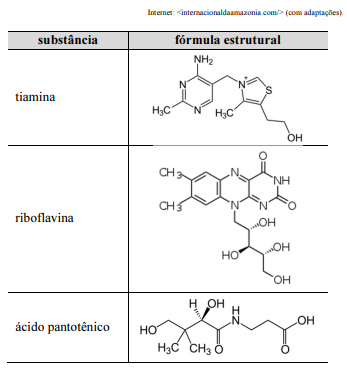
A partir do texto e das fórmulas estruturais mostradas na tabela precedente, julgue o próximo item.
Considerando-se o poli(tereftalato de etileno), um polímero de condensação obtido pela esterificação de um monômero com o etilenoglicol, e as fórmulas moleculares constantes da tabela a seguir, é correto afirmar que o monômero que reage com o etilenoglicol, para formar o poli(tereftalato de etileno), é o ácido benzoico.
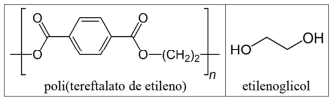

O nome do reagente orgânico presente nessa reação é:
A massa de iodo-131 presente na amostra decairá a 25 mg no seguinte intervalo de tempo, em dias: