Questões de Vestibular Comentadas sobre química
Foram encontradas 1.405 questões
DADOS QUE PODEM SER USADOS NESTA PROVA

Vinho é uma bebida alcoólica, geralmente produzida por fermentação do sumo da uva. Quando o vinho azeda, ocorre a seguinte reação química:
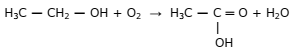
Sobre essa reação, é correto dizer que
DADOS QUE PODEM SER USADOS NESTA PROVA

A seguir encontram-se duas descrições incompletas de experimentos realizados em um laboratório de química. Assinale a opção que completa correta e respectivamente essas descrições.
Enchendo-se um tubo de ensaio com ¾ de ___________ 1 e adicionando-se algumas tiras de zinco, bolhas de ___________2 formam-se imediatamente.
Ao colorir 2 mL de solução de ___________3 com uma gota de solução de fenoftaleína, e em seguida despejar-se esta solução em 5 mL de ___________ 4 , observa-se que a cor ___________. 5
DADOS QUE PODEM SER USADOS NESTA PROVA

O vinagre é uma solução aquosa de ácido acético, largamente utilizado na culinária em saladas e outros pratos. Nos produtos comerciais, vem indicada, no rótulo, a porcentagem do ácido acético presente, em termos de massa do ácido por volume de vinagre. Atente para as seguintes afirmações sobre o ácido acético.
I. O ácido acético pertence à função orgânica dos ácidos carboxílicos e, pela nomenclatura IUPAC, é denominado de ácido etanoico.
II. A representação da fórmula estrutural do ácido
acético é: 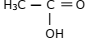
Considerando as proposições acima apresentadas, é
correto afirmar que
DADOS QUE PODEM SER USADOS NESTA PROVA

Isomeria plana ocorre quando a diferença entre os isômeros pode ser explicada por fórmulas estruturais planas. Considerando esse conceito, analise as seguintes afirmações:
I. No pentano existem três isômeros de cadeia.
II. São encontrados quatro isômeros de posição no penteno.
III. No éter constituído por 5 átomos de carbono existem dois isômeros de compensação (ou metameria).
É correto o que se afirma em
DADOS QUE PODEM SER USADOS NESTA PROVA

As baterias recarregáveis possuem a característica de prolongar muito sua vida útil, o que aumenta a relação custo-benefício. A bateria recarregável mais conhecida é a bateria de chumbo usada nos carros, que, por armazenar energia elétrica, é definida como bateria de armazenamento. Esse tipo de bateria consiste em seis células, cada uma gerando 2,0 V para um total de 12,0 V. A reação celular geral é dada pela seguinte equação química:
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l)
Sobre essa reação, é correto afirmar que
DADOS QUE PODEM SER USADOS NESTA PROVA

Várias substâncias com as quais temos contato em nossa vida cotidiana possuem carbonos quirais (carbonos assimétricos), como, por exemplo, o açúcar nos alimentos, a isomeria na celulose do papel e o ácido lático encontrado no organismo humano. Considerando as formas quirais, atente para os seguintes compostos:
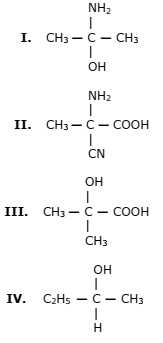
Dos compostos acima apresentados, os que podem
existir nas formas quirais são somente os que
constam em
Considere a seguinte reação:
A + B → butanoato de etila + H2O
Nessas condições, A e B são, respectivamente:
Uma amostra de uma rocha de massa 0.250 g, com baixo teor de Cr, foi submetida à fusão com Na2O2 transformando o cromo em cromato (CrO4 = ). A amostra foi dissolvida em água em ebulição, acidificada e o CrO4 = foi convertido a dicromato (Cr2O7 = ). Na sequência, a amostra foi titulada com 27 mL de solução de Fe2+. Os produtos desta reação foram Fe3+ e Cr3+. Numa padronização paralela, 47 mL de Fe2+ foram usados na redução de 0.1172 g de K2Cr2O7. A reação decorrente foi:
Cr2O7 = + 6Fe2+ + 14H+ → 2Cr3+ + 6Fe3+ + 7H2O.
A massa percentual de Cr na amostra é:
O volume em mL (cm3 ) de uma solução de HNO3 de densidade 1.497 g/cm3 , contendo 93.25% por peso de HNO3 puro, necessários para atacar, completamente, uma esfera de cobre com 2.0 cm de diâmetro, é:
Dados: Volume da esfera: V = (4/3)πR3 , π = 3.14, densidade (Cu) = 8.9 g/cm3
Reação que ocorre: Cu + 4HNO3(conc.) → Cu(NO3)2 + 2H2O + 2NO2
O pH de uma solução que contém um precipitado de Cr(OH)3 (Kps = 6.0 x 10-11 a uma dada temperatura) deve ser ajustado de modo que todo o precipitado se dissolva, produzindo uma solução na qual a [Cr3+] seja 0.1 mol/L.
Nesse caso, o valor do pH é de, aproximadamente:
Dado: Kw = 1.0x 10-14
O cátion Ba2+ pode apresentar toxicidade aos humanos, dependendo de sua concentração e forma química. Por exemplo, BaSO4 é pouco tóxico, sendo usado como contraste radiológico, por ser insolúvel em solução aquosa, enquanto BaCO3 e Ba(NO3)2 são muito tóxicos, pois liberam Ba2+ no organismo. Em um laboratório foram feitos dois testes de solubilidade para identificar o conteúdo de três frascos não rotulados que poderiam ser de Ba(NO3)2, BaCO3 ou BaSO4. Os resultados dos dois testes de solubilidade são apresentados a seguir.
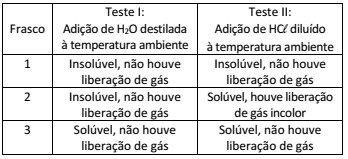
Considerando os ensaios realizados, indique quais são os
compostos contidos nos frascos 1, 2 e 3, respectivamente.
O hidróxido de alumínio (Al(OH)3), ao precipitar em solução aquosa, forma um sólido gelatinoso que pode ser usado como agente floculante no tratamento de água. Essa precipitação pode ocorrer pela adição de um hidróxido solúvel a uma solução aquosa ácida contendo um sal de alumínio solúvel, como o AlCl3. Entretanto, adicionando-se excesso de hidróxido ao meio, há a formação de íons Al(OH)4− , espécie solúvel em água, e o precipitado se solubiliza novamente. Dessa forma, dependendo do pH do meio, uma dentre as espécies Al(OH)4 −(aq), Al(OH)3(s) e Al 3+(aq) estará presente na solução em quantidade maior que as demais, como exemplificado no esquema.
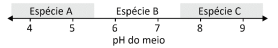
A alternativa que mostra corretamente qual das espécies estará
em quantidade maior que as duas outras em cada faixa de pH é:
Um marcador radioativo (24Na) foi injetado em um ponto de um cano de água subterrâneo e, na sequência, com um detector sobre o solo, foi medida a radioatividade ao longo do percurso do cano. A figura a seguir esquematiza o local de injeção do marcador e o perfil da radioatividade detectada ao longo do cano.
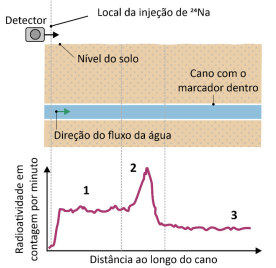
Assinale a alternativa que melhor explica o perfil da radioatividade.
Note e adote:
Tempo de meia-vida do 24Na = 15 horas.
Cálculos renais, conhecidos popularmente por “pedras nos rins”, consistem principalmente em oxalato de cálcio, CaC2O4, espécie cuja constante de solubilidade (Kps) é de aproximadamente 2 × 10−9 . Os íons oxalato, presentes em muitos vegetais, reagem com os íons cálcio para formar oxalato de cálcio, que pode gradualmente se acumular nos rins. Supondo que a concentração de íons cálcio no plasma sanguíneo seja de cerca de 5 × 10−3 mol/L, qual seria a concentração mínima, em mol/L, de íons oxalato para que CaC2O4 precipitasse?
Note e adote:
Desconsidere a presença de quaisquer
outros íons e considere que a
concentração no plasma é determinante
para a precipitação do oxalato.
As reações de hidrólise de ésteres, quando realizadas em meio aquoso, podem ser catalisadas pela adição de ácido, sendo a reação mais lenta em meios próximos da neutralidade.
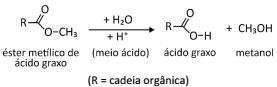
Duas reações idênticas para a hidrólise desse éster foram
realizadas nas mesmas condições, variando apenas o pH do
meio: uma delas foi conduzida em pH=2 e outra em pH=6. Qual
dos seguintes diagramas representa de forma mais adequada a
quantidade de ácido graxo formada em função do tempo de
reação para as hidrólises em pH=2 e pH=6?
Oxigênio (O2) e ozônio (O3) estão em constante processo de consumo e produção na estratosfera, como representado pelas equações químicas a seguir. As reações I e II ilustram etapas da produção de ozônio a partir de oxigênio, e a reação III mostra a restauração de oxigênio a partir de ozônio.
Reação ΔH (kcal/mol de O2)
I O2 → 2 O. −118
II 2 O2 + 2 O. → 2 O3 ΔHII
III 2 O3 → 3 O2 +21
Uma das formulações para os adesivos “silicones” usados na construção civil é chamada de “silicone acético”. Essa nomenclatura é utilizada porque o componente ativo libera ácido acético durante a formação do precursor, espécie que promoverá a polimerização, como representado genericamente a seguir.
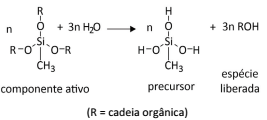
Considerando essas informações, qual dos componentes
ativos a seguir faria com que a formulação fosse considerada
como “silicone acético”?
A produção do vidro tem por base a modificação da estrutura cristalina do quartzo (SiO2) por meio do seu aquecimento e da adição de óxidos alcalinos, dentre eles o Na2O. Esse processo adiciona cátions sódio à estrutura do quartzo, tornando-a amorfa. Alguns vidros, como os utilizados em telas de smartphones, passam ainda por processo de troca iônica para aumentar a resistência a quedas e riscos. Para isso, o vidro é banhado em uma solução salina contendo íons potássio. Dessa forma, o potássio substitui o sódio na estrutura, sem que o volume do vidro se altere.
Com base nessas informações, é correto afirmar que os íons
potássio