Questões de Vestibular
Sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 385 questões
Para essas espécies químicas, constata-se que

Uma
das consequências do aumento do dióxido de carbono na atmosfera é a
acidificação dos oceanos. Naturalmente, tem-se o equilíbrio químico entre o
dióxido de carbono da atmosfera e o dissolvido nos oceanos. Com o aumento de
dióxido de carbono nas águas oceânicas esse equilíbrio é perturbado, e, logo,
organismos vivos constituídos, principalmente, de carbonato de cálcio, são
prejudicados.
Sobre o aumento da acidez nos oceanos e as suas
consequências, analise as proposições.
I. A
acidificação dos oceanos ocorre devido à reação química entre o gás carbônico
dissolvido e a água, resultando na formação do ácido carbônico cuja fórmula
química é HCO3.
II. Os
íons carbonatos provenientes do equilíbrio do carbonato de cálcio reagem com os
íons H+ gerados pelo ácido carbônico,
a fim de compensar o excesso de acidez gerado no oceano.
III. O
caráter mais ácido dos oceanos favorece a descalcificação dos exoesqueletos dos
corais, assim como dificulta a formação de novas estruturas de carbonato de
cálcio.
Assinale
a alternativa correta.
Instrução: Leia atentamente o texto abaixo para responder a questão.


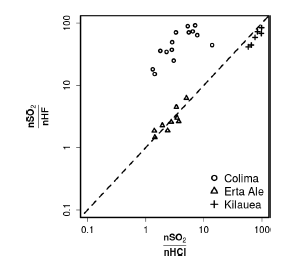
De acordo com a figura, em relação às quantidades de gases dissolvidos no magma, é correto afirmar que as concentrações de SO2 são maiores que as de HF e de HCl
Em um experimento, os tubos I, II, III e IV, cujas aberturas estão totalmente vedadas, são iluminados por luzes de mesma potência, durante o mesmo intervalo de tempo, mas com cores diferentes. Além da mesma solução aquosa, cada tubo possui os seguintes conteúdos:
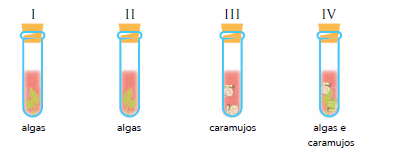
A solução aquosa presente nos quatro tubos tem, inicialmente, cor vermelha. Observe, na escala abaixo, a relação entre a cor da solução e a concentração de dióxido de carbono no tubo.
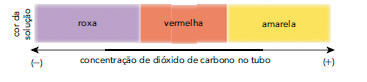
Os tubos I e III são iluminados por luz amarela, e os tubos II e IV por luz azul. Admita que a espécie de alga utilizada no experimento apresente um único pigmento fotossintetizante. O gráfico a seguir relaciona a taxa de fotossíntese desse pigmento em função dos comprimentos de onda da luz.
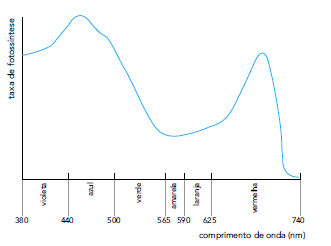
Após o experimento, o tubo no qual a cor da solução se modificou mais rapidamente de vermelha
para roxa é o representado pelo seguinte número:
Não produzir qualquer tipo de resíduo ou poluente é o principal atributo em favor do hidrogênio como combustível para gerar energia elétrica. Ele faz funcionar células de combustível, equipamentos que produzem eletricidade sem danos ambientais. Como uma das fontes de hidrogênio é a água, uma das alternativas, em consonância com a preocupação ambiental, é o reuso da água como produção de energia renovável, utilizando esgotos e efluentes industriais.
O grupo de professores da Escola de Engenharia de São Carlos/USP desenvolveu um método para produzir hidrogênio em um reator de fluxo contínuo, constantemente alimentado com rejeitos que seriam, muitas vezes, descartados sem tratamento em rios e lagoas. No sistema, bactérias anaeróbicas do gênero Clostridium, que não precisam de oxigênio para viver, aderem a partículas de polietileno dentro de um reator.
Nos automóveis, movidos a células de combustível, o consumo de hidrogênio varia de 1,0 a 10,0g/km rodado, segundo um professor do grupo.
(OLIVEIRA, 2009, p. 100).
O método para produzir hidrogênio, a partir de rejeitos descartados, sem tratamento, em rios e lagoas, utiliza bactérias anaeróbicas, do gênero Clostridium, para fermentar material orgânico.
Durante a fermentação, são produzidos hidrogênio, H2(g), metano, CH4(g), sulfeto de hidrogênio, H2S(g), e dióxido de carbono, CO2(g), além de outros produtos. A partir dessas informações, é correto afirmar:
Não produzir qualquer tipo de resíduo ou poluente é o principal atributo em favor do hidrogênio como combustível para gerar energia elétrica. Ele faz funcionar células de combustível, equipamentos que produzem eletricidade sem danos ambientais. Como uma das fontes de hidrogênio é a água, uma das alternativas, em consonância com a preocupação ambiental, é o reuso da água como produção de energia renovável, utilizando esgotos e efluentes industriais.
O grupo de professores da Escola de Engenharia de São Carlos/USP desenvolveu um método para produzir hidrogênio em um reator de fluxo contínuo, constantemente alimentado com rejeitos que seriam, muitas vezes, descartados sem tratamento em rios e lagoas. No sistema, bactérias anaeróbicas do gênero Clostridium, que não precisam de oxigênio para viver, aderem a partículas de polietileno dentro de um reator.
Nos automóveis, movidos a células de combustível, o consumo de hidrogênio varia de 1,0 a 10,0g/km rodado, segundo um professor do grupo.
(OLIVEIRA, 2009, p. 100).
Um laboratório realiza a análise de células utilizando uma solução fisiológica salina com pH neutro. O laboratório dispõe de apenas quatro substâncias que poderiam ser usadas no preparo dessa solução: HCl, NaCl, NaOH e NaHCO3 .
Dentre elas, a que deve ser escolhida para uso na análise está indicada em:
Leia o texto para responder à questão.
Lâmpadas sem mercúrio
Agora que os LEDs estão jogando para escanteio as lâmpadas fluorescentes compactas e seu conteúdo pouco amigável ao meio ambiente, as preocupações voltam-se para as lâmpadas ultravioletas, que também contêm o tóxico mercúrio.
Embora seja importante proteger-nos de muita exposição à radiação UV do Sol, a luz ultravioleta também tem propriedades muito úteis. Isso se aplica à luz UV com comprimentos de onda curtos, de 100 a 280 nanômetros, chamada luz UVC, que é especialmente útil por sua capacidade de destruir bactérias e vírus.
Para eliminar a necessidade do mercúrio para geração da luz UVC, Ida Hoiaas, da Universidade Norueguesa de Ciência e Tecnologia, montou um diodo pelo seguinte procedimento: inicialmente, depositou uma camada de grafeno (uma variedade cristalina do carbono) sobre uma placa de vidro. Sobre o grafeno, dispôs nanofios de um semicondutor chamado nitreto de gálio-alumínio (AlGaN). Quando o diodo é energizado, os nanofios emitem luz UV, que brilha através do grafeno e do vidro.
(www.inovacaotecnologica.com.br. Adaptado.)

DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO QUÍMICO NÚMERO ATÔMICO MASSA ATÔMICA
H 1 1,0
He 2 4,0
Li 3 6,9
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Ne 10 20,2
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Ca 20 40,0
Mn 25 55,0
Co 27 58,9
Zn 30 65,4
Ge 32 72,6
As 33 75,0
Nb 41 93,0
Pb 82 208,0
I. NH4OH
II. H3PO4
III. Ca3 (PO4)2
IV. Ca(OH)2
Sobre os compostos acima, assinale a afirmação correta.
Sobre a obtenção do gás sulfídrico, sua estrutura, suas propriedades e reações, assinale a única afirmação verdadeira.
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
