Questões de Vestibular de Química - Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador
Foram encontradas 270 questões
A figura ilustra a cinética de uma reação química com e sem a presença de catalisador.
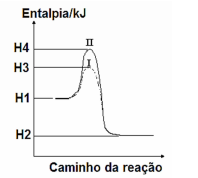
Numere a segunda coluna de acordo com a primeira coluna e, a seguir, assinale a sequência CORRETA encontrada.
1. H1 ( ) Energia liberada pela reação
2. H2 ( ) Energia de ativação da reação catalisada
3. H2-H1 ( ) Energia de ativação da reação não catalisada
4. H3-H1 ( ) Energia dos produtos
5. H4-H1 ( ) Energia dos reagentes
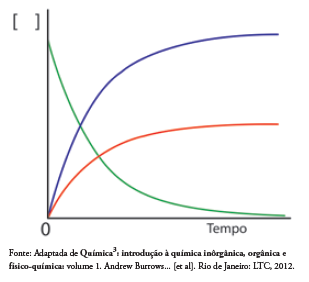
Considerando a reação de decomposição do peróxido de hidrogênio e o gráfico representado ao lado, avalie as afirmativas apresentadas abaixo e assinale a alternativa CORRETA.
I. A curva em verde representa o consumo de peróxido de hidrogênio.
II. A curva em azul representa a produção de oxigênio.
III. A velocidade média de decomposição da água oxigenada pode
ser representada por: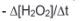
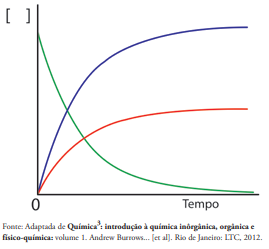
Considerando a reação de decomposição do peróxido de hidrogênio e o gráfico representado abaixo, avalie as afirmativas apresentadas abaixo e assinale a alternativa CORRETA.
I. A curva em verde representa o consumo de peróxido de hidrogênio. II. A curva em azul representa a produção de oxigênio. III. A velocidade média de decomposição da água oxigenada pode ser representada por: -Δ[H2O2]/ Δt