A pressão de vapor de um líquido puro corresponde à pressão exercida por um sistema, mantido em recipiente fechado,
no qual coexistem, em equilíbrio, a fase líquida e o vapor. O valor da pressão de vapor desse sistema está associado,
em grande parte, à natureza e à intensidade das interações entre as moléculas constituintes do líquido, e essa
pressão aumenta com o aumento da temperatura, como mostra, no gráfico, as curvas de pressão de vapor para o
etoxietano, (H
5C
2)
2O, o etanol, C
2H
5OH, e a água, H
2O
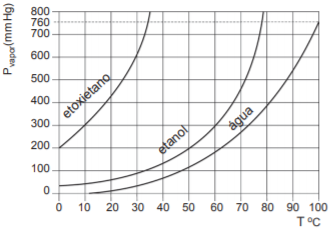
Considerando-se essa informação associada às propriedades físicas dos líquidos puros, é correto afirmar:

