A pressão de vapor de um líquido puro corresponde à pressão ...
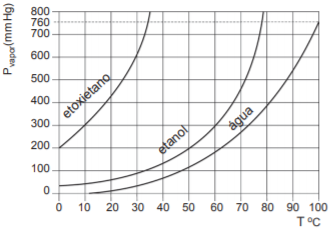
Considerando-se essa informação associada às propriedades físicas dos líquidos puros, é correto afirmar:
- Gabarito Comentado (1)
- Aulas (9)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
A ruptura das interações intermoleculares, no estado líquido, é facilitada pelo aumento da temperatura por ser um processo endotérmico
As forças intermoleculare são forças de atração eletrostática que têm por função realizar a união de moléculas (compostos moleculares), mantendo-as no estado sólido ou líquido. Elas são extremamente importantes, haja vista que determinam todas as propriedades físicas (ponto de fusão, ponto de ebulição, densidade e solubilidade) das substâncias.
a) A pressão de vapor do etanol à temperatura de 70°C é igual ao dobro da pressão exercida pela água, na mesma temperatura.
Errada, a 70 graus o etanol bate mais ou menos ali no 500mmHg já a água bate mais ou menos no 300 mmHg então perceba que não é o dobro
b) O etoxietano entrará em ebulição a uma temperatura maior do que a temperatura de ebulição do etanol, à pressão de 400mmHg.
Errada, o etoxietano entrará em ebulição a uma temperatura menor, lembrando que quanto mais afastada é a curva menor o ponto de ebulição logo a ordem crescente do P.E é etoxietano< etanol< água
c) A ruptura das interações intermoleculares, no estado líquido, é facilitada pelo aumento da temperatura por ser um processo endotérmico.
Correta, quanto maior a temperatura maior a interação fazendo com que uma hora chegue a se romper
d) O valor da temperatura de ebulição da água no alto de uma montanha é maior do que ao nível do mar, que tem a pressão atmosférica de 760mmHg.
Errada, o valor da T.E da água no alto da montanha é menor que no nível do mar
e) A maior volatilidade do etoxietano, em relação a do etanol e a da água, é justificada pela presença das ligações de hidrogênio entre as moléculas do éter.
Errada, se fosse a sim a água também teria maior volatividade pq a água também possui ligações de hidrogênio, lembrando que as ligações de hidrogênios são o FON ( Flúor, Oxigênio e Nitrogênio)
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo