Questões de Vestibular FGV 2016 para Vestibular - Inglês, Física, Química e Língua Portuguesa
Foram encontradas 15 questões

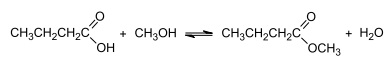 Aroma de maçã
Aroma de maçã Em um teste de laboratório, foram adicionados 10 mol de

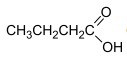 e n mol de CH3OH a um reator de 1 L. O
reator foi fechado e, ao se atingir o equilíbrio reacional, verificou-se a formação de 9 mol, da substância com aroma de
maçã e 9 mol de H2O.
e n mol de CH3OH a um reator de 1 L. O
reator foi fechado e, ao se atingir o equilíbrio reacional, verificou-se a formação de 9 mol, da substância com aroma de
maçã e 9 mol de H2O. Considerando que a constante de equilíbrio referente às condições de temperatura e pressão do processo é K eq = 9, o valor correto da quantidade, em mol, de CH3OH adicionado ao reator é
As2O3 (s) + O2 (g) → As2O5 (s) ΔHor1 = 270 kJ 3 As2O3 (s) + 2 O3 (g) → 3 As2 O5 (s) ΔHor2 = 1096 kJ
Com base nessas informações, é correto afirmar que o valor da entalpia padrão da reação (ΔHor ) de conversão de 1 mol de oxigênio a ozônio, em kJ, é aproximadamente
4 KO2 (s) + 2 CO2 (g) → 2 K2 CO3 (s) + 3 O2 (g)
Em um processo a 27 ºC e 1 atm, são produzidos 1476 L de oxigênio. A quantidade de peróxido de potássio, em kg, mínima para esse processo é aproximadamente
Adote: R = 0,082 atm. L. mol–1 .K–1
É correto afirmar que, entre esses gases poluentes, contribuem diretamente para formação de chuva ácida os gases
O politetrafluoreteno é formado por reação de __________, e a fórmula mínima de seu monômero é ____________.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas.