Questões de Vestibular UERJ 2014 para Vestibular, Segundo Exame - Francês
Foram encontradas 7 questões
O craqueamento é uma reação química empregada industrialmente para a obtenção de moléculas mais leves a partir de moléculas mais pesadas. Considere a equação termoquímica abaixo, que representa o processo utilizado em uma unidade industrial para o craqueamento de hexano.
H3C − CH2 − CH2 − CH2 − CH2 − CH3 (g) ⇌ H3C − CH2 − CH2 − CH3(g) + H2C = CH2 (g) ∆H >0
Em um experimento para avaliar a eficiência desse processo, a reação química foi iniciada sob temperatura T1 e pressão P1 . Após seis horas, a temperatura foi elevada para T2 , mantendo-se a pressão em P1 . Finalmente, após doze horas, a pressão foi elevada para P2 , e a temperatura foi mantida em T2 .
A variação da concentração de hexano no meio reacional ao longo do experimento está
representada em:
Em um experimento, os tubos I, II, III e IV, cujas aberturas estão totalmente vedadas, são iluminados por luzes de mesma potência, durante o mesmo intervalo de tempo, mas com cores diferentes. Além da mesma solução aquosa, cada tubo possui os seguintes conteúdos:
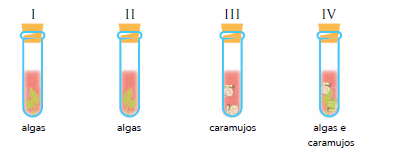
A solução aquosa presente nos quatro tubos tem, inicialmente, cor vermelha. Observe, na escala abaixo, a relação entre a cor da solução e a concentração de dióxido de carbono no tubo.
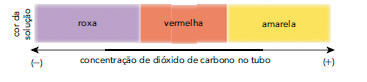
Os tubos I e III são iluminados por luz amarela, e os tubos II e IV por luz azul. Admita que a espécie de alga utilizada no experimento apresente um único pigmento fotossintetizante. O gráfico a seguir relaciona a taxa de fotossíntese desse pigmento em função dos comprimentos de onda da luz.
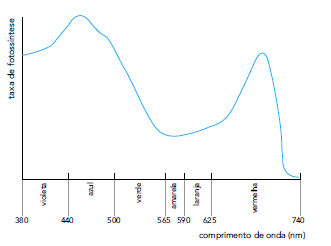
Após o experimento, o tubo no qual a cor da solução se modificou mais rapidamente de vermelha
para roxa é o representado pelo seguinte número: