Questões de Vestibular UFCG 2009 para Vestibular - Primeira Etapa - Dia 1
Foram encontradas 10 questões
A reação é dada por:
Onde R: CH3 ou C2H5, R1: grupo alquila.
O excesso de metanol utilizado no processo de produção de biodiesel pode constituir um problema ambiental, por isso precisa ser purificado para ser reutilizado no processo. Identifique dentre as figuras a mais adequada para o processo de purificação do metanol:
Com base no esquema ao lado, qual é a quantidade de álcool que poderá ser recuperada em 16 horas de produção, tomando por base que a recuperação seja total?
Considerando a tabela abaixo,
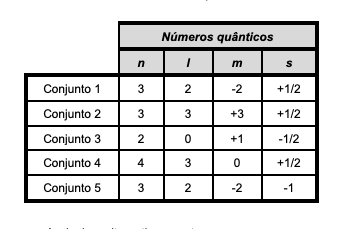
Assinale a alternativa correta.
Considerando a seguinte série de equações químicas propostas e fazendo o balanceamento destas equações,
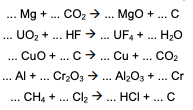
é INCORRETO afirmar que:
Os combustíveis usuais são misturas de hidrocarbonetos que variam com a origem geográfica do petróleo utilizado e dos processos de refino aplicados. De fato, a mistura só pode ser comercializada se ela verifica características estritas sobre as propriedades físicas (densidade, volatilidade), energéticas (poder calórico) e químicas (índice de octanagem, limitação dos teores em certos componentes). Para determinar as propriedades energéticas dos combustíveis, um hidrocarboneto padrão serve como modelo. Para a gasolina, a referência é o octano C8H18.
Em um motor, é a reação de combustão da gasolina que fornece a energia necessária ao seu funcionamento. A energia liberada é proveniente do rearranjo das ligações químicas, conforme mostra a figura abaixo. O ciclo termodinâmico abaixo permite encontrar o valor de ΔrHo .
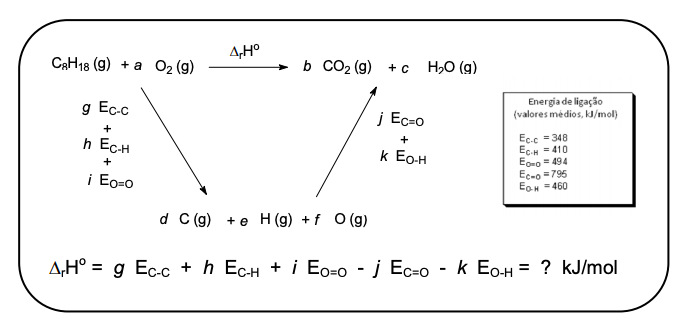
Considerando o ciclo termodinâmico acima e após o balanceamento das reações, indique com V as alternativas corretas e com F as alternativas falsas.
( ) A energia de combustão do octano é de –5.009,0 kJ/mol.
( ) A energia necessária para formar todas as ligações do gás carbônico produzido durante a reação de combustão do octano é de –6.360,0 kJ/mol.
( ) A energia necessária para formar todas as ligações da água produzida durante a reação de combustão do octano é de –4.140,0 kJ/mol.
( ) A energia necessária para quebrar todas as ligações do octano é de +10.164,0 kJ/mol.
( ) A energia necessária para a quebra de todas as ligações dos reagentes consumidos durante a reação de combustão do octano é +16.339,0 kJ/mol.
Assinale a alternativa que indique a sequência exata:
No oceano atlântico, a concentração dos íons sódio Na+ é 0,5 mol/L. Se uma piscina com as dimensões de comprimento 50 m, largura 12 m e profundidade 3 m, for preenchida com a água deste oceano e em seguida 9/10 do seu conteúdo for esvaziado e substituído com água destilada, pode-se concluir que a nova quantidade de íons Na+ na piscina e a nova concentração em íons sódio são respectivamente:
Dados: R = 0,082 atm.L/mol.K
Um técnico foi encarregado de fornecer a estrutura possível de um composto pesquisado, contudo, foi perdida uma parte dos resultados, tendo ele recuperado apenas as seguintes informações:
1) o composto é um cicloalcano que possui grupos alquila (metila, etila e terc-butila) sem se saber o número exato de cada grupo;
2) o composto possui como fórmula molecular: C14H28;
3) o composto possui 3 átomos de carbono classificados como terciários e 2 átomos de carbono classificados como quaternários.
A partir de destas informações, o técnico escreveu várias estruturas possíveis conforme a figura abaixo.
Dentre as cinco estruturas propostas pelo técnico, quantas são corretas, isto é, satisfazem as três informações iniciais?