Poluentes como óxidos de enxofre e de nitrogênio presentes n...
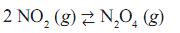
Quando esse recipiente é colocado em um banho de água e gelo, o gás torna- se incolor. Em relação a esse sistema, são feitas as seguintes afirmações:
I. A reação no sentido da formação do gás incolor é exotérmica.
II. Com o aumento da pressão do sistema, a cor castanha é atenuada.
III. Quando o sistema absorve calor, a cor castanha é acentuada.
Dentre as afirmações, as corretas são:
Comentários
Veja os comentários dos nossos alunos
Quando esse recipiente é colocado em um banho de água e gelo
reação exotérmica
I- Se coloca no gelo e ele se torna incolor é porque a reação é exotérmica, então essa ta correta.
II- A pressão é inversamente proporcional ao volume, então, com o aumento da pressão do sistema, o equilíbrio desloca-se para o lado de menor volume, que é o do produto(tem somente 1 mol enquanto o reagente tem 2), então o incolor é atenuado, e não a cor castanha, como diz a questão.
III- Quando o sistema absorve calor, ele ta sendo Endotérmico pelo aumento da temperatura, ou exotérmico por ter absorvido o calor e agora estar mais frio??????
atenuada é antônimo de acentuada
Basta entender a reação:
Diminuição da temperatura (colocar na água com gelo): favorece gás transparente (N2O2).
Portanto: 2NO2 --> N2O2 + energia (exotérmica neste sentido)
I) Correto, como definido na reação acima: 2NO2 --> N2O2 + energia (exotérmica neste sentido)
II) Correto. Com o aumento da pressão no sistema, a reação favorecida será a de menor volume.
Relação de volume é: 2 mol NO2 : 1 mol N2O2
Portanto, o lado favorecido será o de menor volume que é o gás N2O2 (transparente).
III) Correto. Com o aumento da temperatura, o sistema favorece a reação endotérmica.
Conforme defini no início: 2NO2 <-- N2O2 + energia (endotérmica neste sentido)
Conclui-se, portanto, que a reação favorecida será no sentido do 2NO2 (castanho).
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo