O nitrogênio é o elemento mais abundante da atmosfera e faz...
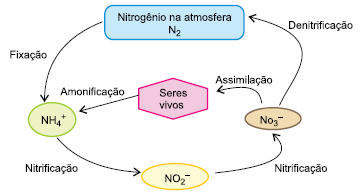
No ciclo do nitrogênio, a etapa que envolve oxidação é a
- Gabarito Comentado (1)
- Aulas (2)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
NO3-: NOXN = - 1 + 6 = + 5
Gabarito do Professor: Letra B.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
Esta questão abrange o conceito de oxidação química. A oxidação acontece quando a substância perde elétrons, e, consequentemente, há um aumento no número de oxidação (NOX). Sendo assim, é preciso procurar nas alternativas a que representa uma etapa em que o NOX do nitrogênio aumenta. É importante saber que o NOX do oxigênio é, na maioria das vezes, -2, enquanto que o do hidrogênio é +1. Sendo assim, é possível saber como varia o NOX do nitrogênio (NOXN) nas etapas:
• Fixação:
N2 → NH4+
N2: NOX = 0, substância simples
NH4+: NOX do composto = +1, NOX do H = +1, logo: NOXN + 4 ∙ 1 = + 1 ∴ NOXN = 1 - 4 = -3
• Nitrificação:
NH4+ → NO2-
NH4+: NOXN = -3
NO2-: NOX do composto = -1, NOX do O = -2, logo: NOXN - 2 ∙ 2 = - 1 ∴ NOXN = - 1 + 4 = +3
NO2- → NO3-
NO2-: NOXN = +3
NO3-: NOX do composto = -1, NOX do O = -2, logo: NOXN - 3 ∙ 2 = - 1 ∴ NOXN = - 1 + 6 = +5
• Denitrificação:
NO3- → N2
NO3-: NOXN = - 1 + 6 = + 5
N2: NOX = 0, substância simples
Com base no exposto, analisemos as alternativas:
A) INCORRETA - Na etapa de denitrificação, o NOX do nitrogênio varia de +5 a 0. Logo, o NOX diminuiu, o que significa que o nitrogênio ganhou elétrons e sofreu redução, e não oxidação.
B) CORRETA - Na etapa de nitrificação, o NOX do nitrogênio varia de -3 a +3, para que o NH4+ forme NO2-. Dessa forma, o NOX aumenta, o que significa que o nitrogênio perdeu elétrons e sofreu oxidação. São envolvidos 6 mols de elétrons na reação, pois o NOX do nitrogênio variou de -3 a +3.
C) INCORRETA - Na etapa de fixação, o NOX do nitrogênio varia de 0 a -3, ou seja, o NOX diminuiu, o que indica que o nitrogênio ganhou elétrons e sofreu redução, e não oxidação.
D) INCORRETA - Como dito na alternativa C, na etapa de fixação, o nitrogênio não sofre oxidação.
E) INCORRETA - Na etapa de nitrificação, o NOX do nitrogênio varia de +3 a +5, para que o NO2- forme NO3-. Dessa forma, o NOX aumenta, o que significa que o nitrogênio perdeu elétrons e sofreu oxidação. São envolvidos 2 mols de elétrons na reação, pois o NOX do nitrogênio variou de +3 a +5.
Gabarito do Professor: Letra B.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo