A figura representa um experimento de coleta de 0,16 g de gá...
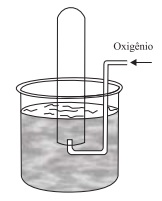
Quando o nível da água dentro do tubo de ensaio é o mesmo que o nível de fora, a pressão no interior do tubo é de 0,86 atm. Dadas a pressão de vapor (H2O) a 27 °C = 0,040 atm e R = 0,082 atm·L·K–1 ·mol –1 , o volume de gás, em mL, dentro do tubo de ensaio é igual a
- Gabarito Comentado (1)
- Aulas (4)
- Comentários (1)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
Pela Lei de Dalton, temos que:
PT = PO2 + PH2O,
Logo, PO2 = PT – PH2O
PO2 = 0,86 – 0,04 = 0,82 atm.
Então, PO2VT = NO2RT
0,82VT = 0,16 . 0,082. 300 / 32
VT = 0,15 L ou 150 Ml
Opção correta C.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
Pt=Po2-PH2O
Pt=0,86-0,04 = 0,82
M do O2: 32 molar
m do O2: 0,16 g
n=m/M
n=0,16/32= 0,005
P * V=n *r * t
0,82 * V= 0,005* 0,082 * 300
0,82*V= 0,123
V=0,123/0,82
V=0,15 --- 150 L
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo