Na tabela a seguir, é reproduzido um trecho da classificação...
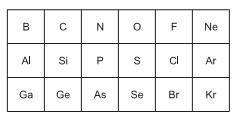
A partir da análise das propriedades dos elementos, está correto afirmar que
- Gabarito Comentado (1)
- Aulas (7)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
A eletronegatividade na tabela periódica cresce nos períodos de acordo com o aumento do número atômico e com a diminuição do número de camadas na família. Assim, a ordem decrescente de eletronegatividade é F, O, N, Cl, Br, I, S, C, P, H. Assim, o nitrogênio é um dos elementos mais eletronegativos que o fósforo.
Opção correta C.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
Resolução:
O átomo do elemento nitrogênio (N) possui apenas 2 camadas
eletrônicas (2o Período), portanto, em comparação com o
fósforo (P), que é um elemento da mesma família do
nitrogênio (VA ou 15), mas possui 3 camadas eletrônicas
(3o Período), conclui-se que o nitrogênio deve ser mais
eletronegativo que o fósforo.
Lembre-se que:
H P C S I Br Cl N O F
——————————————————
ordem crescente de eletronegatividade
Alternativa C
a) a afinidade eletrônica do neônio é maior que a do flúor.- Errada, na eletroafinidade nem os gases nobres entra
b) o fósforo apresenta maior condutividade elétrica que o alumínio.- Errada, é o contrário
c) o nitrogênio é mais eletronegativo que o fósforo.- Correta, Lembre se da sequência de eletronegatividade F, O ,N, Cl, Br, I, S, C, P, H BIZU: Fui Ontem No Clube Briguei I Sai Correndo Pro Hospital, logo perceba que sim o Nitrogênio é mais eletronegativo do que o Fosfóro lembrando que essa sequência aumenta da direita para esquerda.
d) a primeira energia de ionização do argônio é menor que a do cloro.- Errada, lembre se que a energia de ionização ou o potencial de ionização aumenta de baixo pra cima e da esquerda para direita portanto perceba que o Ar está do lado do cloro o que faz com que sua energia de ionização seja menor que a do cloro portanto falsa alternativa
e) o raio do íon Al 3+ é maior que o do íon Se 2– Errada, pelo motivo de que O raio atômico dos ânions é maior do que dos cátions.
cátion < átomo neutro < ânion
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo