Questões de Vestibular Comentadas por alunos sobre equilíbrio químico em química
Foram encontradas 277 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Na tabela abaixo estão descritos alguns dados de três ácidos inorgânicos de Bronsted-Lowry:
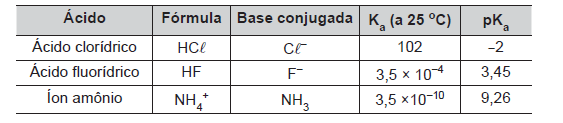
Em relação aos três ácidos acima e suas bases conjugadas, assinale a afirmação correta:
Uma das reações utilizadas para a demonstração de deslocamento de equilíbrio, devido à mudança de cor, é a representada pela equação a seguir:
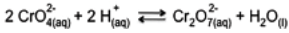
sendo que, o cromato (CrO42- ) possui cor amarela e o dicromato (Cr2O72- ) possui cor alaranjada.
• Sobre esse equilíbrio foram feitas as seguintes afirmações:
I. A adição de HCl provoca o deslocamento do equilíbrio para a direita.
II. A adição de NaOH resulta na cor alaranjada da solução.
III. A adição de HCl provoca o efeito do íon comum.
IV. A adição de dicromato de potássio não desloca o equilíbrio.
• As afirmações corretas são:
Os gases hidrogênio e bromo foram colocados para reagir, até o equilíbrio ser atingido, segundo a equação abaixo.
H2(g) + Br2(g) ⇌ 2 HBr(g) ; ΔH° < 0
A tabela a seguir tem duas colunas, uma que indica um tipo de perturbação do equilíbrio e outra que indica a situação final do equilíbrio restabelecido.
Perturbação do equilíbrio
I – aumento da temperatura
II – aumento da pressão pela diminuição do volume do reator
III – adição de catalisador
IV – adição de Br2(g)
Situação final do equilíbrio restabelecido
P – aumento da concentração
de HBr(g)
Q – aumento da concentração de Br2(g)
R – sem alteração signifi cativa das concentrações de equilíbrio
A associação CORRETA de perturbação e situação final do equilíbrio restabelecido é indicada na alternativa
O incêndio na boate Kiss, em Santa Maria (RS), ocorrido no início deste ano [2013], trouxe à tona uma série de questões sobre a segurança dos estabelecimentos e também sobre o atendimento a vítimas de grandes incêndios. Uma delas é por que foi preciso trazer dos Estados Unidos uma substância tão simples – uma vitamina B injetável – para atender os pacientes que, segundo exames, foram intoxicados com cianeto?

O gás cianídrico liberado na queima da espuma, utilizada para melhorar a acústica da casa noturna, intoxicou a maior parte das vítimas, segundo perícia.
“É descaso e ignorância”, resume o toxicologista Anthony Wong, diretor do Ceatox (Centro de Assistência Toxicológica do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo). Segundo ele, é inadmissível que o país não tenha a substância e que seu uso não seja difundido entre médicos e socorristas, como acontece em outras partes do mundo.
A hidroxocobalamina, que faz parte do complexo B, é usada em altas concentrações como antídoto para o cianeto. O gás, o mesmo que já foi usado no extermínio de judeus nos campos de concentração nazistas, é subproduto da queima de diversos componentes usados na indústria, como o plástico, o acrílico e a espuma de poliuretano. Segundo os peritos que investigam o incêndio em Santa Maria, essa última foi usada no isolamento acústico da boate.
Capaz de matar em poucos minutos, o cianeto bloqueia a cadeia respiratória das células, impedindo que o oxigênio chegue aos órgãos e tecidos. Quando usada logo após a exposição, a hidroxocobalamina salva vidas. “O efeito é tão rápido que parece até milagroso”, conta Wong. Mas isso não é algo que os médicos aprendem na escola: “São poucas as faculdades que oferecem curso de toxicologia e, nas que tem, a matéria é opcional”.
(noticias.uol.com.br. Adaptado.)
Informações adicionais:
• O gás cianídrico é o cianeto de hidrogênio (HCN) no estado gasoso.
• A fórmula estrutural da hidroxocobalamina é:

• A massa molar da hidroxocobalamina é aproximadamente igual
a 1,3 × 10³g/mol.

