Questões de Vestibular
Foram encontradas 873 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
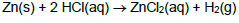
Se 10,00 g de Zn foram misturados com 8,00 g de ácido clorídrico, quantos mols de H2 foram liberados aproximadamente:
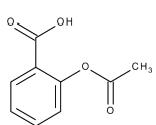
Dados: C = 12,0; H = 1,0; O = 16,0 g/mol. A concentração, em mol/L, de AAS na solução é
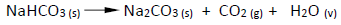
A termólise de 84 g do reagente produzirá a massa de carbonato de sódio e o número de mols de dióxido de carbono iguais a, respectivamente,
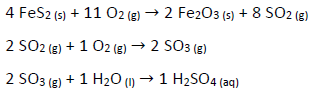
Considere as afirmações: I. O pentóxido de vanádio é um catalisador heterogêneo no meio reacional. II. Os altos valores de temperatura e pressão levam ao aumento das colisões efetivas, o que diminui a energia de ativação. III. A formação de dióxido de enxofre consiste em uma reação de oxirredução, em que o oxigênio sofre oxidação, e o enxofre, redução.
Está correto o que se afirma em