Questões de Vestibular
Foram encontradas 410 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
NaCℓO → Na+ + CℓO–
CℓO– + H2O
O número de oxidação do cloro no íon hipoclorito e a condição ideal para aumentar a concentração desse íon na solução são
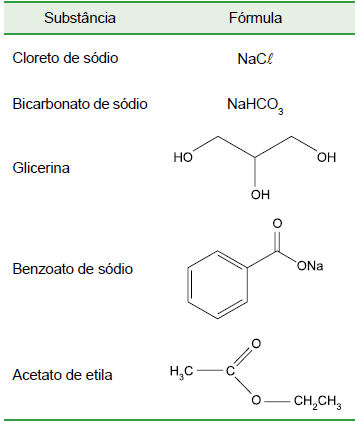
A substância presente na tabela que possui composição adequada para atuar como umectante é
As lacunas do texto são, correta e respectivamente, preenchidas por:
Considere a tabela para responder à questão

2 SO2(g) + O2(g) ⇌2 SO3(g)
Sabendo que, reagindo 12 mols de SO2 e 12 mols de O2 foram produzidos 8 mols do SO3 em um recipiente de 1,0 L, qual a constante de equilíbrio da reação (Kc)?