Questões de Vestibular Comentadas por alunos sobre representação das transformações químicas em química
Foram encontradas 437 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
ANO INTERNACIONAL DA TABELA PERIÓDICA
Há 150 anos, a primeira versão da tabela periódica foi elaborada pelo cientista Dimitri Mendeleiev. Trata-se de uma das conquistas de maior influência na ciência moderna, que reflete a essência não apenas da química, mas também da física, da biologia e de outras áreas das ciências puras. Como reconhecimento de sua importância, a UNESCO/ONU proclamou 2019 o Ano Internacional da Tabela Periódica.
Na tabela proposta por Mendeleiev em 1869, constavam os 64 elementos químicos conhecidos até então, além de espaços vazios para outros que ainda poderiam ser descobertos. Para esses possíveis novos elementos, ele empregou o prefixo “eca”, que significa “posição imediatamente posterior”. Por exemplo, o ecassilício seria o elemento químico a ocupar a primeira posição em sequência ao silício no seu grupo da tabela periódica.
Em homenagem ao trabalho desenvolvido pelo grande cientista, o elemento químico artificial de número
atômico 101 foi denominado mendelévio.
Considere uma amostra laboratorial de 0,43 g de mendelévio.
O número de átomos presentes nessa amostra equivale a:
Com o reflorestamento, é possível minimizar os efeitos do aquecimento global, tendo em vista que uma árvore consegue captar, em média, 15,6 kg do CO2 lançado na atmosfera por ano. Sabe-se que, na combustão completa da gasolina, todos os átomos de carbono são convertidos em moléculas de CO2.
Admitindo que 1 litro de gasolina contém 600 g de isoctano (C8H18) e 200 g de etanol (C2H6O), no período de 1 ano, uma árvore será capaz de captar o CO2 emitido na combustão completa de x litros de gasolina.
O valor de x corresponde, aproximadamente, a:
O Cardanol é um fenol obtido do líquido da castanha de caju (LCC), a partir do processo de aquecimento a que as castanhas são submetidas para fins alimentícios, de modo a romper a casca externa e liberar o óleo.
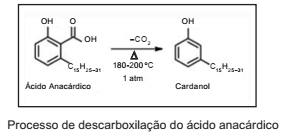
Sendo o LCC um subproduto de agronegócio do caju e
correspondente a, aproximadamente, 25% do peso da castanha, supõe-se que 5% desse líquido seja o ácido anacárdico. Assim, para produzir 5.96 toneladas de Cardanol,
supondo que sua massa molar seja de aproximadamente,
298 g/mol, a quantidade necessária de castanhas em toneladas é de:
O TBT (M.M = 291 g/mol) é um composto polar, hidrofóbico e lipofílico que foi introduzido no mercado nos anos 40. É componente de tintas anti-incrustantes, utilizadas em cascos de barcos, redes e jaulas de aquacultura a fim de impedir a fixação de organismos como algas e invertebrados (mexilhão, cracas, etc.). Além disso, o TBT é utilizado também na agricultura como pesticida, conservante de madeiras e, numa escala menor, em desinfetantes e em tratamentos algicidas em materiais de construção. A sua elevada difusão no meio marinho tornou-se uma preocupação ambiental em nível mundial. Atualmente, é considerada a substância mais tóxica produzida pelo homem.
A composição centesimal do TBT é de 49.49% de Carbono, 9.62% de Hidrogênio e 40.89% de Estanho e sua fórmula molecular é:


