Questões de Vestibular
Foram encontradas 638 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Bicarbonato de sódio e carbonato de sódio são duas substâncias químicas muito presentes no cotidiano. Entre várias aplicações, o bicarbonato de sódio é utilizado como antiácido estomacal e fermento de pães e bolos, e o carbonato de sódio, conhecido como barrilha ou soda, tem sua principal aplicação na fabricação de vidro comum.
As fórmulas químicas do bicarbonato de sódio e do carbonato de sódio estão correta e respectivamente representadas em
Alguns metais são imprescindíveis para o bom funcionamento do organismo humano. Os denominados oligoelementos, normalmente são encontrados em pequenas quantidades e, quando presentes em excesso, podem ser prejudiciais à saúde.
A Doença de Wilson, por exemplo, é caracterizada pelo acúmulo de um metal não prateado, que, se liberado na corrente sanguínea, pode resultar na formação de um anel de coloração escura no olho do indivíduo.
Assinale a alternativa que indica, respectivamente, o metal e o órgão do portador da Doença de Wilson onde ele se acumula antes de ser liberado para a corrente sanguínea.
A queima de combustíveis fósseis é uma fonte de dióxido de enxofre atmosférico, assim como as erupções vulcânicas, como a que ocorreu recentemente na Islândia.
Considere ainda o equilíbrio químico, representado pela equação, que ocorre na água de uma piscina, na qual se utiliza hipoclorito em seu tratamento:
Cl2(g) + 2OH–(aq) ↔ ClO– (aq) + Cl–(aq) + H2O(l)
Analise as seguintes afirmações:
I. A queima dos combustíveis carvão mineral, petróleo e álcool de cana-de-açúcar é responsável pela maioria das emissões de SO2 no planeta.
II. Acredita-se que a presença na estratosfera de partículas muito finas formadas a partir do SO2 contribua para o resfriamento da Terra, por bloquear parte da radiação solar.
III. A alteração do pH da chuva pode resultar na formação de um gás sufocante em piscinas localizadas em regiões altamente poluídas pelas emissões de SO2 .
São corretas as afirmações:
A cal, muito utilizada na construção civil, é obtida na indústria a partir da reação de decomposição do calcário, representada pela equação:
CaCO3(s) 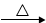 CaO(s) + CO2(g)
CaO(s) + CO2(g)
A fonte de calor para essa decomposição pode ser o gás natural,cuja reação de combustão é representada por:
CH4(g) + 2O2(g) → 2H2O(l) + CO2(g)
Considerando as massas molares:
H = 1,0 g·mol–1 , C = 12,0 g·mol–1 ,
O = 16,0 g·mol–1 , Ca = 40,0 g·mol–1 ,
a massa de gás carbônico lançada na atmosfera quando são produzidos
560 kg de cal, a partir da decomposição térmica do calcário,
utilizando o gás natural como fonte de energia, é:
