Questões de Vestibular Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 341 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A equação química a seguir indica que há participação de gases na reação.
2C (sólido) + O2 (g) −→ 2CO(g)
Considere que, em um primeiro momento, a reação ocorra sem expansão de volume (volume constante) em um sistema fechado a 27 ◦C e que o valor do calor medido seja de 52600 cal.
Se essa mesma reação ocorrer a pressão constante, assinale a alternativa que apresenta, corretamente, o calor liberado, em cal.
(Dado: R = 2 cal/K)
 + 3O2(g) → 2CO2 (g) + 3H2O
+ 3O2(g) → 2CO2 (g) + 3H2O  ΔH = - 1366,8kJ
ΔH = - 1366,8kJ + 25/2 O2(g) → 8 CO2(g) + 9 H2O
+ 25/2 O2(g) → 8 CO2(g) + 9 H2O  ΔH = –5 461,0 kJ
ΔH = –5 461,0 kJDadas as entalpias de formação dos compostos:
CO2(g) ΔHf = - 393 kJ/mol
H2O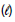 ΔHf = - 286 kJ/mol
ΔHf = - 286 kJ/mol
conclui-se, corretamente, que a entalpia de formação do combustível presente em I é, em kJ/mol,
A2 + B2 → 2 AB
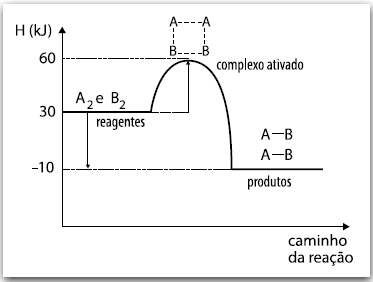
A análise do gráfico permite concluir corretamente que
2 H2(g) + O2(g) → 2 H2O(g) ∆H= - 483,6 kJ
A reação acima é uma reação:
Acerca dessas informações, assinale a alternativa incorreta.