Questões de Vestibular Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 341 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dado:

A reação de hidrogenação do etileno ocorre com aquecimento, na presença de níquel em pó como catalisador. A equação termoquímica que representa o processo é
C2 H4 (g) + H2 (g) → C2 H6 (g) ΔHθ = - 137 kJ.mol-1
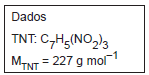
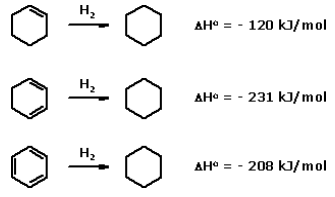
A diferença nas entalpias de hidrogenação das reações apresentadas pode ser explicada pela
