Questões ENEM de Química
Foram encontradas 484 questões
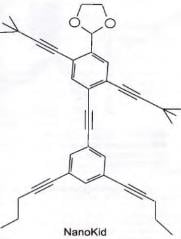
CHANTEAU, S. H.; TOUR, J. M. The Journal of Organic Chemistry. v. 68, n. 23. 2003 (adaptado).
Em que parte do corpo do NanoKid existe carbono quaternário?
Cl2 (g) + 2 H2O ( l ) ⥨ HCIO (aq) + H3O+ (aq) + Cl (aq)
HCIO (aq) + H2O (I) ⥨ H3O+ (aq) + CIO- (aq) pKa = - log Ka = 7,53
A ação desinfetante é controlada pelo ácido hipocloroso, que possui um potencial de desinfecção cerca de 80 vezes superior ao ânion hipoclorito. O pH do meio é importante, porque influencia na extensão com que o ácido hipocloroso se ioniza.
Para que a desinfecção seja mais efetiva, o pH da água a ser tratada deve estar mais próximo de
Para que se consiga atrair um maior número de abelhas para uma determinada região, a molécula que deve estar presente em alta concentração no produto a ser utilizado é:
Em um medicamento, a varfarina é administrada por via intravenosa na forma de solução aquosa, com concentração de 3,0 mg/mL. Um indivíduo adulto, com volume sanguíneo total de 5,0 L, será submetido a um tratamento com solução injetável desse medicamento.
Qual é o máximo volume da solução do medicamento que pode ser administrado a esse indivíduo, pela via intravenosa, de maneira que não ocorram hemorragias causadas pelo anticoagulante?
4 FeS2 (s) + 15O2 (g) + 2 H2O (I) ➙ 2 Fe2(SO4)3 (aq) + 2 H2 SO4 (aq)
FIGUEIREDO, B. R. Minérios e ambiente. Campinas: Unicamp, 2000.
Para corrigir os problemas ambientais causados por essa drenagem, a substância mais recomendada a ser adicionada ao meio é o