Questões do Enem
Comentadas sobre transformações químicas e energia em química
Foram encontradas 68 questões
Atualmente, soldados em campo, seja em treinamento ou em combate, podem aquecer suas refeições, prontas e embaladas em bolsas plásticas, utilizando aquecedores químicos, sem precisar fazer fogo. Dentro dessas bolsas existe magnésio metálico em pó e, quando o soldado quer aquecer a comida, ele coloca água dentro da bolsa, promovendo a reação descrita pela equação química:
Mg (s) + 2 H2O (I) → Mg(OH)2 (s) + H2 (g) + 350 kJ
O aquecimento dentro da bolsa ocorre por causa da
O ferro metálico é obtido em altos-fornos pela mistura do minério hematita (α-Fe2O3) contendo impurezas, coque (C) e calcário (CaCO3), sendo estes mantidos sob um fluxo de ar quente que leva à queima do coque, com a temperatura no alto-forno chegando próximo a 2 000 °C. As etapas caracterizam o processo em função da temperatura.
Entre 200 °C e 700 °C:
3 Fe2O3 + CO → 2 Fe3O4 + CO2
CaCO3 → CaO + CO2
Fe3O4 + CO → 3 FeO + CO2
Entre 700 °C e 1 200 °C:
C + CO2 → 2 CO
FeO + CO → Fe + CO2
Entre 1 200 °C e 2 000 °C:
Ferro impuro se funde
Formação de escória fundida (CaSiO3)
2 C + O2 → 2 CO
BROWN, T L.; LEMAY, H. E.; BURSTEN, B. E. Química: a ciência central. São Paulo: Pearson Education, 2005 (adaptado).
No processo de redução desse metal, o agente redutor é o
A invenção do LED azul, que permite a geração de outras cores para compor a luz branca, permitiu a construção de lâmpadas energeticamente mais eficientes e mais duráveis do que as incandescentes e fluorescentes. Em um experimento de laboratório, pretende-se associar duas pilhas em série para acender um LED azul que requer 3,6 volts para o seu funcionamento. Considere as semirreações de redução e seus respectivos potenciais mostrados no quadro.

Qual associação em série de pilhas fornece diferença de potencial, nas condições-padrão, suficiente para acender o LED azul?
A técnica do carbono-14 permite a datação de fósseis pela medição dos valores de emissão beta desse isótopo presente no fóssil. Para um ser em vida, o máximo são 15 emissões beta/(min g). Após a morte, a quantidade de 14C se reduz pela metade a cada 5 730 anos.
A prova do carbono 14. Disponível em: http://noticias.terra.com.br. Acesso em: 9 nov. 2013 (adaptado).
Considere que um fragmento fóssil de massa igual a 30 g foi encontrado em um sítio arqueológico, e a medição de radiação apresentou 6 750 emissões beta por hora. A idade desse fóssil, em anos, é
A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
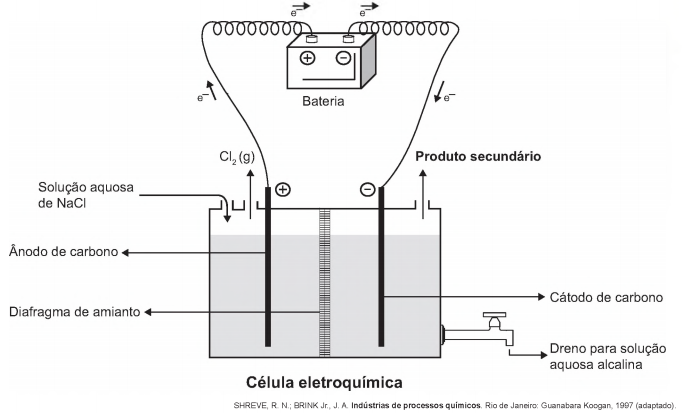
No processo eletrolítico ilustrado, o produto secundário obtido é o
A energia nuclear é uma alternativa aos combustíveis fósseis que, se não gerenciada de forma correta, pode causar impactos ambientais graves. O princípio da geração dessa energia pode se basear na reação de fissão controlada do urânio por bombardeio de nêutrons, como ilustrado:
235U + n → 95Sr + 139Xe + 2 n + energia
Um grande risco decorre da geração do chamado lixo atômico, que exige condições muito rígidas de tratamento e armazenamento para evitar vazamentos para o meio ambiente.
Esse lixo é prejudicial, pois
O ambiente marinho pode ser contaminado com rejeitos radioativos provenientes de testes com armas nucleares. Os materiais radioativos podem se acumular nos organismos. Por exemplo, o estrôncio-90 é quimicamente semelhante ao cálcio e pode substituir esse elemento nos processos biológicos.
FIGUEIRA, R. C. L.; CUNHA, I. I. L. A contaminação dos oceanos por radionuclídeos antropogênicos. Química Nova na Escola, n. 1, 1998 (adaptado).
Um pesquisador analisou as seguintes amostras coletadas em uma região marinha próxima a um local que manipula o estrôncio radioativo: coluna vertebral de tartarugas, concha de moluscos, endoesqueleto de ouriços-do-mar, sedimento de recife de corais e tentáculos de polvo.
Em qual das amostras analisadas a radioatividade foi
menor?
A obtenção do alumínio dá-se a partir da bauxita (Al2O3 .3H2O), que é purificada e eletrolisada numa temperatura de 1 000 °C. Na célula eletrolítica, o ânodo é formado por barras de grafita ou carvão, que são consumidas no processo de eletrólise, com formação de gás carbônico, e o cátodo é uma caixa de aço coberta de grafita.
A etapa de obtenção do alumínio ocorre no
Utensílios de uso cotidiano e ferramentas que contêm ferro em sua liga metálica tendem a sofrer processo corrosivo e enferrujar. A corrosão é um processo eletroquímico e, no caso do ferro, ocorre a precipitação do óxido de ferro(III) hidratado, substância marrom pouco solúvel, conhecida como ferrugem. Esse processo corrosivo é, de maneira geral, representado pela equação química:
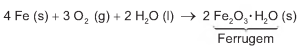
Uma forma de impedir o processo corrosivo nesses
utensílios é
TEXTO I
Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais. Em uma biocélula microbiológica, bactérias catalisam reações de oxidação de substratos orgânicos. Liberam elétrons produzidos na respiração celular para um eletrodo, onde fluem por um circuito externo até o cátodo do sistema, produzindo corrente elétrica. Uma reação típica que ocorre em biocélulas microbiológicas utiliza o acetato como substrato.
AQUINO NETO, S. Preparação e caracterização de bioanodos para biocélula a combustível etanol/O2. Disponível em: www.teses.usp.br. Acesso em: 23 jun. 2015 (adaptado).
TEXTO II
Em sistemas bioeletroquímicos, os potenciais padrão (E°) apresentam valores característicos. Para as biocélulas de acetato, considere as seguintes semirreações de redução e seus respectivos potenciais:
2 CO2 + 7 H+ + 8 e- → CH3COO- + 2 H2O E°’ = -0,3 V
O2 + 4 H+ + 4 e- → 2 H2O E°' = 0,8 V
SCOTT, K.; YU, E. H. Microbial electrochemical and fuel cells: fundamentals and
applications. Woodhead Publishing Series in Energy, n. 88, 2016 (adaptado).
O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada por ferro metálico sob altas temperaturas, conforme a equação química:
3 C2H2 (g) → C6H6 (l)
A energia envolvida nesse processo pode ser calculada indiretamente pela variação de entalpia das reações de combustão das substâncias participantes, nas mesmas condições experimentais:
I. C2H2 (g) + 5/2 O2 (g) → 2 CO2 (g) + H2O (l) ΔHc° = -310 kcal/mol
II. C6H6 (l) + 15/2 O2 (g) → 6 CO2 (g) + 3 H2O (l) ΔHc° = -780 kcal/mol
A variação de entalpia do processo de trimerização, em kcal, para a formação de um mol de benzeno é mais próxima de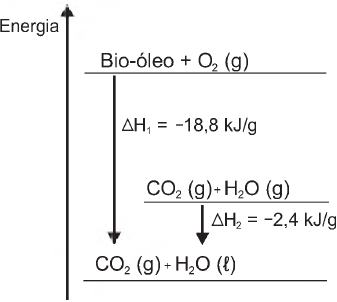
A variação de entalpia, em kJ, para a queima de 5 g desse bio-óleo resultando em CO2 (gasoso) e H2O (gasoso) é:

A equação química que representa a reação de formação da mancha avermelhada é:
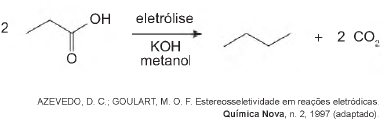
Com base nesse processo, o hidrocarboneto produzido na eletrólise do ácido 3,3-dimetil-butanoico é
ANDRADE, C. D. Poesia completa e prosa. Rio de Janeiro: Aguilar, 1973 (fragmento).
Nesse fragmento de poema, o autor refere-se à bomba atômica de urânio. Essa reação é dita “em cadeia" porque na

Das espécies apresentadas, a adequada para essa recuperação é
SACKS. O. Tio Tungstênío; memórias de uma infância química. São Paulo: Cia, das Letras, 2002.
O fragmento do romance de Oliver Sacks relata a separação dos elementos que compõem a água. O princípio do método apresentado é utilizado industrialmente na
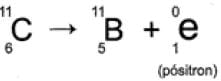
A partir da injeção de glicose marcada com esse nuclídeo, o tempo de aquisição de uma imagem de tomografia é de cinco meias-vidas.
Considerando que o medicamento contém 1,00 g do carbono-1 1 , a massa, em miligramas, do nuclídeo restante, após a aquisição da imagem, é mais próxima de
Suponha que, em um processo de recuperação de cobre puro, tenha-se eletrolisado uma solução de sulfato de cobre (II) (CuS04) durante 3 h, empregando-se uma corrente elétrica de intensidade igual a 10 A. A massa de cobre puro recuperada é de aproximadamente
Dados: Constante de Faraday F= molar 96 500 C/mol; Massa molar em g/mol: Cu= 63,5.
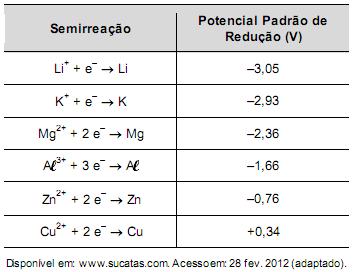
Com base no texto e na tabela, que metais poderiam entrar na composição do anel das latas com a mesma função do magnésio, ou seja, proteger o alumínio da oxidação nos fornos e não deixar diminuir o rendimento da sua reciclagem?