Questões do Enem
Sobre transformações químicas em química
Foram encontradas 73 questões
TiO2 + 2 Cl2 + 2 CO
 TiCI4 + 2 CO2
TiCI4 + 2 CO2 A segunda operação consiste na redução do tetracloreto de titânio, utilizando magnésio metálico:
2 Mg + TiCl4
 2 MgCl2 + Ti
2 MgCl2 + Ti Considere as massas molares:
Cl = 35,5 g/mol ; Ti = 48 g/mol .
Qual a massa de gás cloro necessária para produzir 480 kg de titânio metálico?

Na condição de razão ar/combustível igual a 18, haverá uma emissão
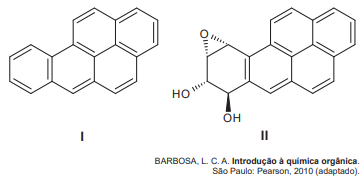
A biotransformação do composto (I) em (II) corresponde a uma reação de
Essa prática popular encontra respaldo no pensamento científico, uma vez que o doce realmente poderá azedar em razão da
2 NaN3 (s) → 2 Na (s) + 3 N2 (g)
O gás produzido tem função de inflar o airbag. Esse tipo de dispositivo contém, aproximadamente, 100 g de NaN3 .
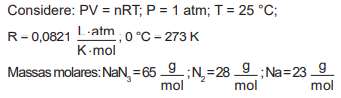
Nesse dispositivo, o volume de gás produzido, em litro, é
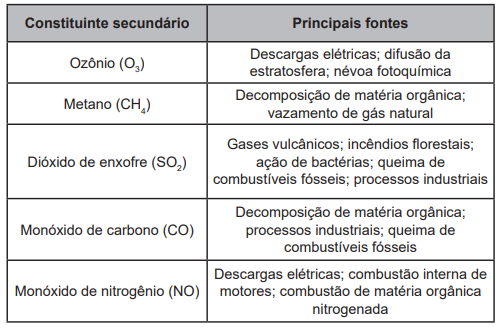
Pode-se reduzir as concentrações de um desses constituintes gasosos secundários na atmosfera pela passagem dos gases através de purificadores químicos contendo uma pasta de calcário, cujo principal constituinte é o CaCO3 , sendo o gás removido por sua conversão em um sal (composto iônico sólido).
SPIRO, T. G.; STIGLIANI, W. M. Química ambiental. São Paulo: Pearson Prentice Hall, 2009 (adaptado). BROWN, L.; LeMAY, H. E.; BURSTEN, B. E. Química: a ciência central. São Paulo: Pearson Prentice Hall, 2005 (adaptado).
Entre os constituintes secundários apresentados, qual pode ser removido pela ação desse purificador químico?
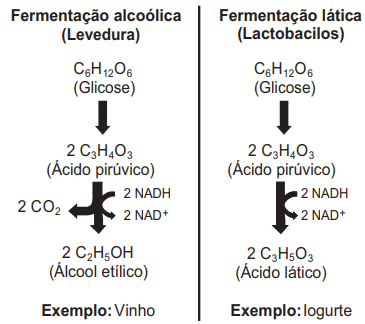
Esses processos de fermentação têm em comum a
ZVEIBIL, V. Z. et al. Cartilha de limpeza urbana. Disponível em: www.ibam.org.br. Acesso em: 6 jul. 2015 (adaptado).
Suponha um frasco metálico de um aerossol de capacidade igual a 100 mL, contendo 0,1 mol de produtos gasosos à temperatura de 650 °C, no momento da explosão.
Considere: R = 0,082 L . atm / mol . K
A pressão, em atm, dentro do frasco, no momento da explosão, é mais próxima de
O urânio é empregado como fonte de energia em reatores nucleares. Para tanto, o seu mineral deve ser refinado, convertido a hexafluoreto de urânio e posteriormente enriquecido, para aumentar de 0,7% a 3% a abundância de um isótopo específico — o urânio-235.
Uma das formas de enriquecimento utiliza a pequena diferença de massa entre os hexafluoretos de urânio-235 e de urânio-238 para separá-los por efusão, precedida pela vaporização. Esses vapores devem efundir repetidamente milhares de vezes através de barreiras porosas formadas por telas com grande número de pequenos orifícios. No entanto, devido à complexidade e à grande quantidade de energia envolvida, cientistas e engenheiros continuam a pesquisar procedimentos alternativos de enriquecimento.
ATKINS, P; JONES, L. Princípios de química: questionando a vida moderna e o meio ambiente. Porto Alegre: Bookman, 2006 (adaptado).
Considerando a diferença de massa mencionada entre os dois isótopos, que tipo de procedimento alternativo ao da
efusão pode ser empregado para tal finalidade?
Os riscos apresentados pelos produtos dependem de suas propriedades e da reatividade quando em contato com outras substâncias. Para prevenir os riscos devido à natureza química dos produtos, devemos conhecer a lista de substâncias incompatíveis e de uso cotidiano em fábricas, hospitais e laboratórios, a fim de observar cuidados na estocagem, manipulação e descarte. O quadro elenca algumas dessas incompatibilidades, que podem levar à ocorrência de acidentes.
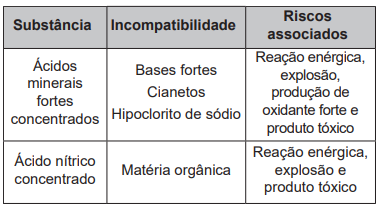
Considere que houve o descarte indevido de dois conjuntos de substâncias:
(1) ácido clorídrico concentrado com Cianeto de potássio;
(2) ácido nítrico concentrado com sacarose.
Disponível em: www.fiocruz.br. Acesso em: 6 dez 2017 (adaptado).
O descarte dos conjuntos (1) e (2) resultará, respectivamente, em
A figura ilustra de solos esquematicamente um processo de remediação de solos contaminados com tricloroeteno (TCE), um agente desengraxante. Em razão de vazamentos de tanques de estocagem ou de manejo inapropriado de resíduos industriais, ele se encontra presente em águas subterrâneas, nas quais forma uma fase líquida densa não aquosa (DNAPL) que se deposita no fundo do aquífero. Essa tecnologia de descontaminação emprega o Íon persulfato (S2O82-), que é convertido no radical •SO4- por minerais que contêm Fe(Ill). O esquema representa de forma simplificada o mecanismo de ação química sobre o TCE e a formação dos produtos de degradação.
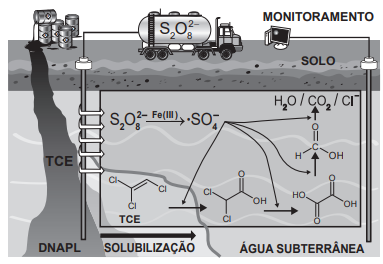
Esse procedimento de remediação de águas subterrâneas baseia-se em reações de
O elemento iodo (I) tem função biológica e é acumulado na tireoide. Nos acidentes nucleares de Chernobyl e Fukushima, ocorreu a liberação para a atmosfera do radioisótopo 131I, responsável por enfermidades nas pessoas que foram expostas a ele. O decaimento de uma massa de 12 microgramas do isótopo 131I foi monitorado por 14 dias, conforme o quadro.
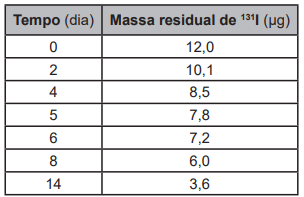
Após o período de 40 dias, a massa residual desse
isótopo é mais próxima de
Um grupo de alunos realizou um experimento para observar algumas propriedades dos ácidos, adicionando um pedaço de mármore (CaCO3) a uma solução aquosa de ácido clorídrico (HCl), observando a liberação de um gás e o aumento da temperatura.
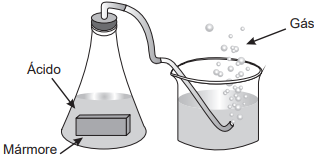
O gás obtido no experimento é o:
Supondo a queima completa de 100 g de carvão antracito, a massa de gás liberada na atmosfera é, em grama, mais próxima de
4 FeS2 (s) + 15 O2 (g) + 2 H2 O (l) → 2 Fe2 (SO4 )3 (aq) + 2 H2 SO4 (aq)
Um dos processos de intervenção nesse problema envolve a reação do resíduo ácido com uma substância básica, de baixa solubilidade em meio aquoso, e sem a geração de subprodutos danosos ao meio ambiente.
FIGUEIREDO, B. R. Minérios e ambientes. Campinas: Unicamp, 2000.
Esse processo de intervenção é representado pela equação química:
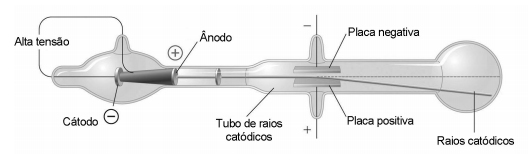
CHANG, R.; GOLDSBY, K. A. Química. Porto Alegre: Bookman, 2013 (adaptado).
Essa radiação invisível detectada nas ampolas é constituída por
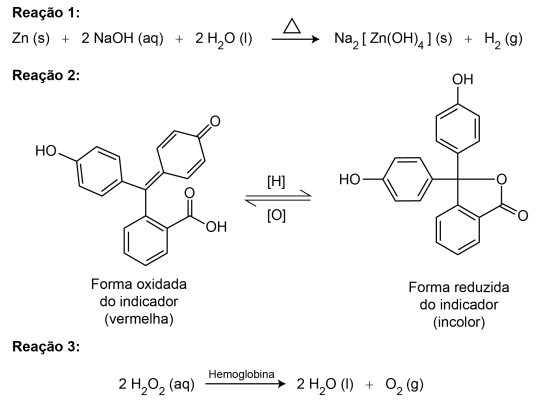
DIAS FILHO, C. R.; ANTEDOMENICO, E. A perícia criminal e a interdisciplinaridade no ensino de ciências naturais. Química Nova na Escola, n. 2, maio 2010 (adaptado).
A mudança de coloração que indica a presença de sangue ocorre por causa da reação do indicador com o(a)
A diferença de emissão de CO2 dos carros desse fabricante em relação ao limite estabelecido na União Europeia é
O perfil de um processo que segue todos os princípios desse ramo da química pode ser representado por:
C2H5OH (I) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g)
Foram analisadas as emissões de CO2 envolvidas em dois veículos, um movido a etanol e outro elétrico, em um mesmo trajeto de 1.000 km.
CHIARADIA, C. A. Estudo da viabilidade da implantação de frotas de veículos elétricos e híbridos elétricos no atual cenário econômico, político, energético e ambiental brasileiro. Guaratinguetá: Unesp. 2015 (adaptado).
A quantidade equivalente de etanol economizada, em quilograma, com o uso do veículo elétrico nesse trajeto, é mais próxima de