Questões Militares
Sobre cinética e cálculo de reatores em engenharia química e química industrial
Foram encontradas 31 questões
Um reator em batelada é usado para operação em pequena escala, para testar novos processos que não tenham sido desenvolvidos completamente, para a fabricação de produtos caros e para processos que sejam difíceis de converter em operações contínuas. A respeito de reatores em batelada, analise as afirmativas.
I. Um reator em batelada não tem entrada nem saída de reagentes ou produtos enquanto a reação está ocorrendo.
II. O balanço geral molar resultante para a espécie j é 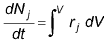 .
.
III. O reator em batelada tem a desvantagem de altas conversões que podem ser obtidas deixando o reagente no reator por longo período de tempo.
Está(ão) correta(s) apenas a(s) afirmativa(s)
Além dos reatores contínuo de tanque agitado, outro tipo de reator comumente usado na indústria é o reator tubular. Sobre os reatores tubulares, informe se as afirmativas abaixo são verdadeiras (V) ou falsas (F) e, em seguida, assinale a alternativa que apresenta a seqüência correta.
( ) Reatores tubulares são usados mais frequentemente para reações em fase líquida.
( ) Os reagentes são continuamente consumidos à medida que eles escoam ao longo do reator.
( ) É normalmente operado em estado estacionário.
A energia das moléculas individuais inclui-se dentro de uma distribuição de energia em que algumas moléculas têm mais energia do que as outras. Esse tipo de distribuição é apresentado na figura a seguir.
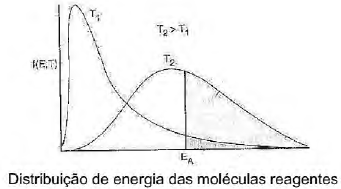
Sobre a distribuição de energia das moléculas reagentes, analise as afirmativas.
I. A função f(E, T) é mais facilmente interpretada identificando-se (f.dE) como a fração de moléculas que tem energia entre E e (E+dE).
II. As moléculas na área sombreada contêm energia cinética suficiente para causar a ruptura das ligações e então ocorrer a reação.
III. À medida que a temperatura diminui, mais moléculas contêm energia suficiente para reagir e a velocidade de reação cresce.
Está(ão) correta(s) apenas a(s) afirmativa(s)

rA = dA = 0,6(A)
dt 0,4 + (A) + 6,2 (A)2
Pretende se reduzir a concentração de A de 2 M para 0,5 M, sendo o fluxo de entrada no reator de 10 L/h (litros/hora). O volume do reator, em litros, considerando as condições de regime permanente, será de
As figuras abaixo se referem a impulsores de fluxo axial com os estabilizadores de direção de fluxo na ponta. Relacione as figuras às suas respectivas características e, em seguida, assinale a alternativa que apresenta a sequência correta.
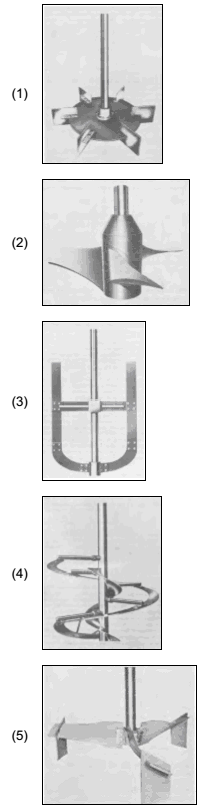
(Foust, A.S et al., 2006)
( ) impulsor de fluxo axial.
( ) impulsor de turbina de aspas planas.
( ) impulsor de fluxo axial para uso em tubos de aspiração.
( ) impulsor helicoidal.
( ) impulsor do tipo âncora.
Preencha as lacunas e, em seguida, assinale a alternativa correta.
O calor padrão da reação CaC2(s) + 5H2O(l) → CaO(s) + 2CO2(g) + 5H2(g) é de 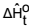 = +69,36 kJ/mol
= +69,36 kJ/mol
A reação é ________________ a 25ºC. O reator deverá ser ________________ para manter a temperatura constante. A energia necessária para quebrar as ligações dos reagentes é ________________ que a energia liberada quando as ligações dos produtos são formados.
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Em sistemas envolvendo reações paralelas, um importante parâmetro é a seletividade (se), definida como a razão entre as taxas de geração dos produtos de interesse (I) e dos secundários (S).
Considere o caso em que a taxa de produção de I é dada por 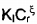 e a de S por
e a de S por 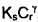 , onde:
, onde:
• Cr é a concentração do reagente;
• KI e Ks são as velocidades específicas de reação para I e S, respectivamente;
• 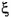 e γ são dois números inteiros e positivos.
e γ são dois números inteiros e positivos.
Para uma temperatura constante, pode-se afirmar que a seletividade: