Questões Militares Sobre engenharia química e química industrial
Foram encontradas 255 questões
xA e xB para as respectivas frações em mol das substâncias A e B na solução líquida,
pA e pB para as respectivas pressões de vapor de A e B no vapor em equilíbrio com a solução líquida, e
p0A e p0B para as respectivas pressões de vapor de A puro e B puro numa mesma temperatura,
I. C(s)+ 2H2(g) -> CH4 (g)
II. N2O(g) -> N2(g) + 1/2 O2 (g)
III. 2NI3 (s) -> N2 (g) + 3I2(g)
IV. 2O3(g) -> 3O2(g)
Assinale a opção que apresenta a(s) reação(ões) química(s) na(s) qual(is) há uma variação negativa de entropia.
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Um gás ideal sofre uma mudança de estado ilustrada pelos gráficos I e II abaixo.
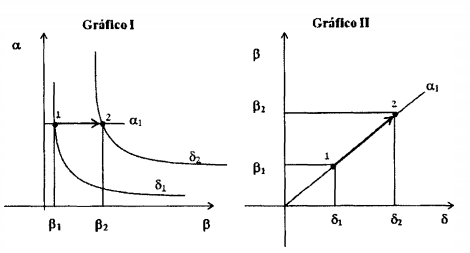
Dentre as alternativas abaixo, assinale aquela que se ajusta aos gráficos acima.
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Em sistemas envolvendo reações paralelas, um importante parâmetro é a seletividade (se), definida como a razão entre as taxas de geração dos produtos de interesse (I) e dos secundários (S).
Considere o caso em que a taxa de produção de I é dada por 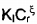 e a de S por
e a de S por 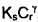 , onde:
, onde:
• Cr é a concentração do reagente;
• KI e Ks são as velocidades específicas de reação para I e S, respectivamente;
• 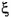 e γ são dois números inteiros e positivos.
e γ são dois números inteiros e positivos.
Para uma temperatura constante, pode-se afirmar que a seletividade:
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Considere a figura a seguir.
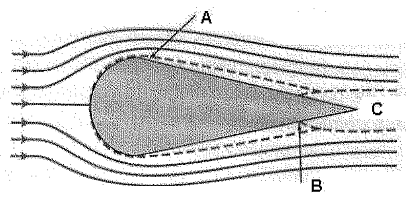
Para o escoamento de ar sobre o objeto carenado apresentado
acima, assinale a opção que identifica corretamente os
pontos A, B e C, respectivamente.
Um sistema em equilíbrio é composto por n0 mol de um gás ideal a pressão P0 , volume V0, temperatura T0 e energia interna U0 . Partindo sempre deste sistema em equilíbrio, são realizados isoladamente os seguintes processos:
I. Processo isobárico de T0 até T0/2 .
II. Processo isobárico de V0 até 2V0 .
III. Processo isocórico de P0 até P0/2 .
IV. Processo isocórico de T0 até 2T0 .
V. Processo isotérmico de P0 até P0/2.
VI. Processo isotérmico de V0 até V0 /2 .
Admitindo que uma nova condição de equilíbrio para esse sistema seja atingida em cada processo x ( x = I, II, III, IV, V e VI), assinale a opção que contém a informação ERRADA.
São descritos abaixo dois experimentos, I e II, nos quais há sublimação completa de uma mesma quantidade de dióxido de carbono no estado sólido a 25 °C:
I - O processo é realizado em um recipiente hermeticamente fechado, de paredes rígidas e indeformáveis.
II - O processo é realizado em cilindro provido de um pistão, cuja massa é desprezível e se desloca sem atrito.
A respeito da variação da energia interna do sistema (ΔU), calor (q) e trabalho (w), nos experimentos I e II, assinale a opção que contém a afirmação ERRADA.

Considere as supostas variações de entropia (∆S) nos processos abaixo:
I) cristalização do sal comum (∆S > 0)
II) sublimação da naftalina (naftaleno ) ( ∆S > 0)
III) mistura de água e álcool ( ∆S < 0)
IV) ferro (s) ferro (l) ( ∆S > 0)
ferro (l) ( ∆S > 0)
V) ar 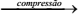 ar comprimido (∆S < 0)
ar comprimido (∆S < 0)
As variações de entropia indicadas nos processos que estão corretas são:
DADOS:
Valores de tangente:
tan(0°) = 0, tan(30°) = (√3)/3, tan(45°) = 1, tan(60°) = √3, tan(90°) = ∞, tan(180°-α) = -tan(α), tan(-α) = -tan(α).
Valores de seno:
sen(0°) = 0, sen(30°) = 1/2, sen(45°) = (√2)/2, sen(60°) = (√3)/2, sen(90°) = 1, sen(90°-α) = cos(α), sen(180°-α) = sen(α), sen(-α) = -sen(α).
Valores de cosseno:
cos(0°) = 1, cos(30°) = (√3)/2, cos(45°) = (√2)/2, cos(60°) = 1/2, cos(90°) = 0, cos(90°-α ) = sen(α), cos(180°-α) = -cos(α), cos(-α) = cos(α).
Transformada de Laplace:
L{f(t)} = F(s), L{exp(-at)} = 1/(s+a), L{1 - exp(-at)} = a/(s(s+a)), L{cos(at)} = s/(s2 +a2 ), L{sen(at)} = a/(s2 +a2).
Resistividade aproximada dos condutores de cobre:
seção transversal de 1,5 mm2 = 10 Ω/km, seção transversal de 2,5 mm2 = 7 Ω/km,
seção transversal de 4 mm2 = 4 Ω/km, seção transversal de 6 mm2 = 3 Ω/km.
Representação de número complexo em forma polar: a∠b onde a é o módulo e b o argumento.
Representação do complemento do valor A: Ā
Um sistema linear invariante no tempo tem a seguinte função característica
s3 + 3 s2 + 3 s + K = 0, onde K é uma variável de controle.
Analise a estabilidade do sistema e assinale a alternativa correta.
DADOS:
Valores de tangente:
tan(0°) = 0, tan(30°) = (√3)/3, tan(45°) = 1, tan(60°) = √3, tan(90°) = ∞, tan(180°-α) = -tan(α), tan(-α) = -tan(α).
Valores de seno:
sen(0°) = 0, sen(30°) = 1/2, sen(45°) = (√2)/2, sen(60°) = (√3)/2, sen(90°) = 1, sen(90°-α) = cos(α), sen(180°-α) = sen(α), sen(-α) = -sen(α).
Valores de cosseno:
cos(0°) = 1, cos(30°) = (√3)/2, cos(45°) = (√2)/2, cos(60°) = 1/2, cos(90°) = 0, cos(90°-α ) = sen(α), cos(180°-α) = -cos(α), cos(-α) = cos(α).
Transformada de Laplace:
L{f(t)} = F(s), L{exp(-at)} = 1/(s+a), L{1 - exp(-at)} = a/(s(s+a)), L{cos(at)} = s/(s2 +a2 ), L{sen(at)} = a/(s2 +a2).
Resistividade aproximada dos condutores de cobre:
seção transversal de 1,5 mm2 = 10 Ω/km, seção transversal de 2,5 mm2 = 7 Ω/km,
seção transversal de 4 mm2 = 4 Ω/km, seção transversal de 6 mm2 = 3 Ω/km.
Representação de número complexo em forma polar: a∠b onde a é o módulo e b o argumento.
Representação do complemento do valor A: Ā
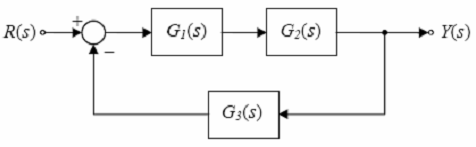
Considere o sistema linear invariante no tempo colocado na figura a seguir, onde as variáveis mostradas foram obtidas por transformada de Laplace. A função de transferência Y(s)/R(s) é