Questões Militares
Sobre física térmica - termologia em física
Foram encontradas 525 questões
Em um recipiente termicamente isolado de capacidade térmica 40,0cal/°C e na temperatura de 25 °C são colocados 600 g de gelo a −10 °C e uma garrafa parcialmente cheia, contendo 2,0L de refrigerante também a 25 °C , sob pressão normal.
Considerando a garrafa com capacidade térmica desprezível e o refrigerante com características semelhantes às da água, isto é, calor específico na fase líquida 1,0 cal /g °C e na fase sólida 0,5 cal /g °C , calor latente de fusão de 80,0 cal /g °C bem como densidade absoluta na fase líquida igual a 1,0g/ cm3 , a temperatura final de equilíbrio térmico do sistema, em °C , é
Com relação à dilatação dos sólidos e líquidos isotrópicos, analise as proposições a seguir e dê como resposta a soma dos números associados às afirmações corretas.
(01) Um recipiente com dilatação desprezível contém certa massa de água na temperatura de 1°C , quando é, então, aquecido lentamente, sofrendo uma variação de temperatura de 6°C . Nesse caso, o volume da água primeiro aumenta e depois diminui.
(02) Quando se aquece uma placa metálica que apresenta um orifício, verifica-se que, com a dilatação da placa, a área do orifício aumenta.
(03) Quando um frasco completamente cheio de líquido é aquecido, este transborda um pouco. O volume de líquido transbordado mede a dilatação absoluta do líquido.
(04) O vidro pirex apresenta maior resistência ao choque térmico do que o vidro comum porque tem menor coeficiente de dilatação térmica do que o vidro comum.
(05) Sob pressão normal, quando uma massa de água é aquecida de 0 °C até 100 °C sua densidade sempre aumenta.
(06) Ao se elevar a temperatura de um sistema constituído
por três barras retas e idênticas de ferro interligadas de
modo a formarem um triângulo isósceles, os ângulos
internos desse triângulo não se alteram.
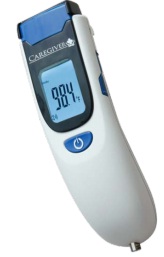
Sabendo que esse termômetro fornece medidas na escala Fahrenheit, a temperatura em graus Celsius, que corresponde ao valor indicado no termômetro da figura é:
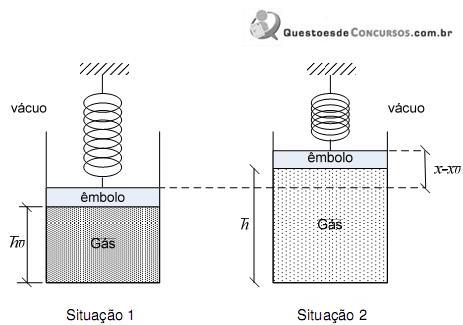
A figura acima mostra um sistema posicionado no vácuo formado por um recipiente contendo um gás ideal de massa molecular M e calor específico c em duas situações distintas. Esse recipiente é fechado por um êmbolo preso a uma mola de constante elástica k, ambos de massa desprezível. Inicialmente (Situação 1), o sistema encontra-se em uma temperatura T0, o êmbolo está a uma altura h0 em relação à base do recipiente e a mola comprimida de x0 em relação ao seu comprimento relaxado.
Se uma quantidade de calor Q for fornecida ao gás (Situação 2), fazendo com que o êmbolo se desloque para uma altura h e a mola passe a estar comprimida de x, a grandeza que varia linearmente com Q é
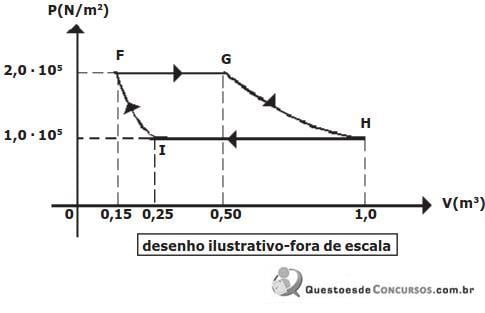
A variação de energia interna sofrida pelo gás na transformação adiabática IF é

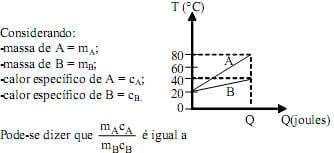
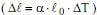 pode-se dizer que o coeficiente de dilatação linear (α) pode possuir como unidade
pode-se dizer que o coeficiente de dilatação linear (α) pode possuir como unidade 
Com base nessas informações, julgue os itens subsequentes.
Considerando que a água esteja presa nos canos, é correto afirmar que a sua pressão aumentará quando a temperatura cair de 4 oC para 3 oC.

Com base nessas informações, julgue os itens subsequentes.
Supondo que, em vez de isolante térmico, haja vácuo entre as paredes interna e externa do coletor, é correto afirmar que não haverá perda de calor pelo fundo da caixa.

Com base nessas informações, julgue os itens subsequentes.
A variação percentual da área da placa ( ) será superior (ΔA / A) 1% quando a sua temperatura subir de 4 oC para 40 oC.
Um gás ideal foi armazenado em um recipiente, formando um sistema fechado com uma pressão inicial (P1), temperatura inicial (T1) e volume inicial (V1). Logo após, foi fornecido calor ao sistema, obtendo-se um novo valor de pressão (P2 = 2P1) e o volume permaneceu constante.
Com base no texto, marque a alternativa que apresenta a razão entre T1 e T2: