Questões Militares de Química - Cinética Química
Foram encontradas 80 questões
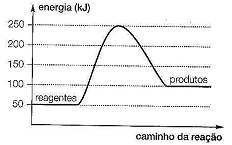
Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?
2NO(g) + O2(g) →2NO2(g) , v = k[NO]2 [O2]
Para esta reação, são propostos os mecanismos reacionais I, II e III com suas etapas elementares de reação:
I. 2NO(g) ⇌ N2O2 (g) equilíbrio rápido
N2O2(g) + O2(g) → 2NO2 (g) lenta
II. NO(g) + O2 (g) ⇌ NO3(g) equilíbrio rápido
NO (g) + NO3 (g) → 2NO2 (g) lenta
III. NO(g) + ½ O2(g) → NO2(g) rápida
NO2(g) + ½ O2(g) ⇌ NO3(g) equilíbrio rápido
NO2(g) + NO3(g) ⇌ N2O4(g) equilíbrio rápido
N2O4(g) → 2NO2 (g) lenta
Dos mecanismos propostos, são consistentes com a lei de velocidade observada experimentalmente
I. Para reações bimoleculares, o fator pré-exponencial na equação de Arrhenius é proporcional à frequência de colisões, efetivas ou não, entre as moléculas dos reagentes.
II. O fator exponencial na equação de Arrhenius é proporcional ao número de moléculas cuja energia cinética relativa é maior ou igual à energia de ativação da reação.
III. Multiplicando-se o negativo da constante dos gases (−R) pelo coeficiente angular da reta ln k versus 1/T obtém-se o valor da energia de ativação da reação.
IV. O fator pré-exponencial da equação de Arrhenius é determinado pela intersecção da reta ln k versus 1/T com o eixo das abscissas.
Das proposições acima, está(ão) ERRADA(S)