Questões Militares de Química - Cinética Química
Foram encontradas 80 questões
Conversores catalíticos de automóveis são utilizados para reduzir a emissão de poluentes. Os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras que aceleram a transformação de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio (genericamente NxOy) em gás nitrogênio (N2) e gás oxigênio (O2). Em relação ao uso de catalisadores e as substâncias citadas no texto, são feitas as seguintes afirmações:
I – As reações de decomposição dos óxidos de nitrogênio a gás oxigênio e a gás nitrogênio ocorrem com variação no número de oxidação das espécies.
II – O CO2 é um óxido ácido que quando reage com a água forma o ácido carbônico.
III – Catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação.
IV – O monóxido de carbono é um óxido básico que ao reagir com a água forma uma base.
V – A molécula do gás carbônico apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas:
Um mineral muito famoso, pertencente ao grupo dos carbonatos, e que dá origem a uma pedra semipreciosa é a malaquita, cuja a fórmula é: Cu2(OH)2CO3 (ou CuCO3.Cu(OH)2).
Experimentalmente pode-se obter malaquita pela reação de precipitação que ocorre entre soluções aquosas de sulfato de cobre II e carbonato de sódio, formando um carbonato básico de cobre II hidratado, conforme a equação da reação:
2 CuSO4 (aq) + 2 Na2CO3 (aq) + H2O (l) → CuCO3.Cu(OH)2 (s) + 2 Na2SO4 (aq) + CO2 (g)
Na reação de síntese da malaquita, partindo-se de 1060 g de carbonato de sódio e considerando-se um rendimento de reação de 90%, o volume de CO2 (a 25 ºC e 1 atm) e a massa de malaquita obtida serão, respectivamente, de:
Dados: – massas atômicas Cu = 64 u; S = 32 u; O = 16 u; Na = 23 u; C = 12 u; H = 1 u.
– volume molar 24,5 L/mol, no estado padrão.
Observe a reação a seguir.
NO2(g) + O3(g) → NO3(g) O2(g)
Dados a 25 °C :
Lei da velocidade: velocidade = k[NO2][O3]
Constante de velocidade (k) : k = 4,4 x 107 dm3 • mol-1 • s-1
[NO2] : concentração de dióxido de nitrogênio (NO2)
[O3] : concentração de ozônio (O3)
A reação química acima ocorre na atmosfera terrestre quando o dióxido de nitrogênio presente no ar poluído entra em contato
com o ozônio. Com relação a este fenômeno químico, é
correto afirmar que:
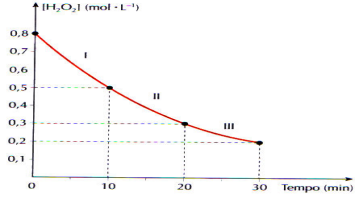 Calcule a velocidade média de decomposição da água
oxigenada, em mol.L-1.min-1, nos intervalos I, II, I e no
intervalo de 0 a 30 min:
Calcule a velocidade média de decomposição da água
oxigenada, em mol.L-1.min-1, nos intervalos I, II, I e no
intervalo de 0 a 30 min: 