Questões Militares de Química - Equilíbrio Químico
Foram encontradas 49 questões
Os corais fixam-se sobre uma base de carbonato de cálcio (CaCO3), produzido por eles mesmos. O carbonato de cálcio em contato com a água do mar e com o gás carbônico dissolvido pode estabelecer o seguinte equilíbrio químico para a formação do hidrogenocarbonato de cálcio:
CaCO3 (s) + CO2 (g) + H2O (l) 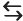 Ca(HCO3)2 (aq)
Ca(HCO3)2 (aq)
Considerando um sistema fechado onde ocorre o equilíbrio químico da reação mostrada acima,
assinale a alternativa correta.
Considere que o pH estomacal seja igual a 2. Quando o fármaco ácido acetilsalicílico (AAS) é ingerido, no estômago sofre ionização em meio aquoso, estabelecendo o seguinte equilíbrio:
AAS(s) + H2O(l)  H3O+(aq) + AAS–(aq) ΔH < 0
H3O+(aq) + AAS–(aq) ΔH < 0
Nessas condições, é CORRETO afirmar que a ionização do AAS é:
(Dados: log 1,49 = 0,17 e log 1,18 = 0,07.)