Questões Militares de Química - Equilíbrio Químico
Foram encontradas 203 questões
São descritos três experimentos (I, II e III) utilizando-se em cada um 30 mL de uma solução aquosa saturada, com corpo de fundo de cloreto de prata, em um béquer de 50 mL a 25 °C e 1 atm:
I. Adiciona-se certa quantidade de uma solução aquosa 1 mol.L−1 em cloreto de sódio.
II. Borbulha-se sulfeto de hidrogênio gasoso na solução por certo período de tempo.
III. Adiciona-se certa quantidade de uma solução aquosa 1 mol.L−1 em nitrato de prata.
Em relação aos resultados observados após atingir o equilíbrio, assinale a opção que apresenta o(s)
experimento(s) no(s) qual(is) houve aumento da quantidade de sólido.
São feitas as seguintes afirmações a respeito dos produtos formados preferencialmente em eletrodos eletroquimicamente inertes durante a eletrólise de sais inorgânicos fundidos ou de soluções aquosas de sais inorgânicos:
I. Em CaCl2 (l) há formação de Ca s) no catodo.
II. Na solução aquosa 1×10-3mol.L −1 −em Na2SO4 há aumento do pH ao redor do anodo.
III. Na solução aquosa 1mol.L−1 em AgNO3 há formação de O2 (g) no anodo.
IV. Em NaBr (l) há formação de Br2 (l) no anodo.
Das afirmações acima, está(ão) ERRADA(S) apenas
A 25 °C, a força eletromotriz da seguinte célula eletroquímica é de 0,45 V: Pt(s)|H2 (g, 1 atm) | H+ ( mol.L-1)|| KCl (0,1 mol.L -1) | Hg2 Cl2 (s) | Hg(l)| Pt (s) Sendo o potencial do eletrodo de calomelano – KCl (0,1 mol.L -1)| Hg2 Cl2 (s)| Hg(l)
– nas condições-padrão
igual a 0,28 V e x o valor numérico da concentração dos íons H+
, assinale a opção com o valor aproximado do
Ag+ (aq) + e-
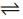 Ag(c); Eo = 0,799 e AgCl (c) + e-
Ag(c); Eo = 0,799 e AgCl (c) + e- 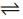 Ag(c) Cl- (aq); E = 0,222 V
Ag(c) Cl- (aq); E = 0,222 Vem que ο Eo é o potencial do eletrodo em relação ao eletrodo padrão de hidrogênio nas condições-padrão.
Considere o produto de solubilidade (K ps), a 25 0C , das substâncias I II e III:
I. Cα (OH)2; K ps = 5,0 × 10 −6II. Mg (OH)2; K ps = 5,6 × 10 −12
III . Zn (OH)2; K ps = 3,0 × 10 −17