Questões Militares de Química - Representação das transformações químicas
Foram encontradas 298 questões
Dada a seguinte equação iônica de oxidorredução:
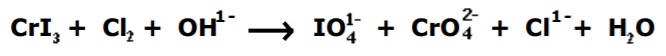
Considerando o balanceamento de equações químicas por oxidorredução, a soma total dos coeficientes mínimos e inteiros obtidos das espécies envolvidas e o(s) elemento(s) que sofrem oxidação, são, respectivamente,
Bicarbonato 100,0
Cálcio 22,0
Sódio 8,98
Nitrato 4,11
Sulfato 6,00
Magnésio 3,26
Potássio 2,70
Cloreto 0,73
Fluoreto 0,34
Sabe-se que a massa molar do íon sulfato (SO42-) é de 96 g/mol. A quantidade de mols de íons sulfato contida em 16 L dessa água mineral é:
Cl2(g) + OH1-(aq) → Cl1-(aq) + ClO31-(aq) + H2O(l)
O carbonato de sódio (Na2CO3) empregado na fabricação de vidro é preparado a partir do carbonato de cálcio (CaCO3) e cloreto de sódio (NaCl), segundo a equação balanceada:
CaCO3 + 2 NaCl → Na2CO3 + CaCl2
Partindo-se de 1250 g de carbonato de cálcio (com grau de pureza de 80%) e 650 g de cloreto de sódio (com grau de pureza de 90%), a massa de carbonato de sódio (Na2CO3) obtida dessa reação, admitindo-se um rendimento da reação de 80%, será de:
Dados:
Massas atômicas: C=12u; O=16u; Na=23u; Cl=35,5u; Ca=40u
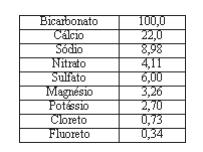
Sabe-se que a massa molar do íon sulfato (SO4 2- ) é de 96 g/mol. A quantidade de mols de íons sulfato contida em 16 L dessa água mineral é: