Questões Militares de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Foram encontradas 75 questões

Com base nessas informações e considerando
 a variação de
a variação deentalpia padrão das reações a 25 ºC, julgue os itens a seguir.
4 C3H5(NO3)3(l) → 6 N2(g) + 12 CO(g) + 10 H2O(g) + 7 O2(g)
Considerando os gases acima como ideais, a temperatura de 300 Kelvin (K) e a pressão de 1 atm, o volume gasoso total que será produzido na detonação completa de 454 g de C3H5(NO3)3(l) é:
Dados:
Elemento H(hidrogênio) C( carbono) O ( Oxigênio) N( nitrogênio)
Massa 1 12 16 14
atômica(u)
Constante universal dos gases: R=8,2 · 10-2 atm · L · K-1 · mol-1
A explosão de 8,8 L de trinitroglicerina (TNG, d = 1,59 g/m L) que ocorreu com 100% de rendimento, pode ser expressa pela equação química a seguir:
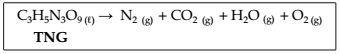
Supondo que todo o gás carbônico produzido possa
ser captado, quantos extintores de incêndio com
capacidade para 2 kg desse gás, poderiam ser
envasados aproximadamente?