Questões Militares de Química - Sistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum.
Foram encontradas 16 questões
H2S = H+ + HS- HS- = H+ + S-2
K1=1,1.10-⁷
K2=10-14
As reações acima representam a ionização do ácido sulfídrico em água. Numa solução de 0,11 M de H2S, quala [H+]?
Uma solução aquosa saturada de gás sulfídrico possui concentração igual a 0,1M e constante de ionização igual a 10-22 Calcule a concentração de sulfeto necessária para precipitação dos cátions do segundo Grupo, sabendo-se que o pH deve ser regulado para se obter uma solução 0,25M em ácido clorídrico, e assinale a opção correta.
Dados: H2S → 2 H+ + S-2
Observe a tabela abaixo.
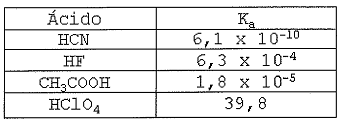
A tabela acima apresenta ácidos com suas respectivas constantes
de ionização (ka) . Assinale a opção que apresenta a
ordem decrescente de ionização desses ácidos.
Em cinco béqueres foram adicionados 50 mL de uma solução de referência, que consiste de uma solução aquosa saturada em cloreto de prata, contendo corpo de fundo, a 25 °C e 1 atm. A cada béquer, foram adicionados 50 mL de uma solução aquosa diluída diferente, dentre as seguintes:
I. Solução de cloreto de sódio a 25 °C.
II. Solução de Glicose a 25 °C.
III. Solução de Iodeto de sódio a 25 °C.
IV. Solução de Nitrato de prata a 25 °C.
V. Solução de Sacarose a 50 °C.
Considere que o corpo de fundo permanece em contato com as soluções após rápida homogeneização das
misturas aquosas e que não ocorre formação de óxido de prata sólido. Nestas condições, assinale a opção que
indica a(s) solução(ões), dentre as acima relacionadas, que altera(m) a constante de equilíbrio da solução de
referência.
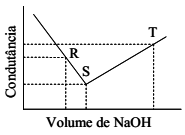
Uma solução aquosa de HCl 0,1 mol L–1 foi titulada com uma solução aquosa de NaOH 0,1 mol L–1. A figura ao lado apresenta a curva de titulação obtida em relação à condutância da solução de HCl em função do volume de NaOH adicionado.
Com base nas informações apresentadas nesta figura, assinale a opção ERRADA.