Questões Militares de Química - Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais.
Foram encontradas 114 questões
Analise as afirmativas abaixo.
I - quando Vb = ½ Ve , pH = pKa .
II - no ponto de equivalência, o pH será > 7,0
III- no ponto de equivalência, o pH será < 7,0
IV- a fenolftaleína (pH 8,0-9,6) pode ser usada como indicador.
V - o vermelho de metila (pH 4, 8-6, 0) pode ser usado como indicador.
Em relação a uma titulação de ácido acético 0,1M com
hidróxido de sódio 0,1M, é correto afirmar que:
Analise a tabela a seguir.
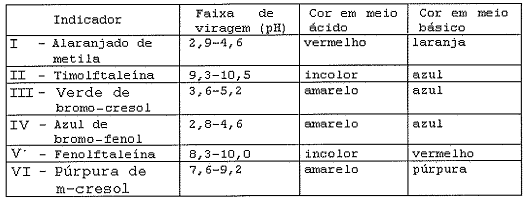
A tabela acima trata de algumas substâncias que podem ser utilizadas como indicadores de neutralização.
Que indicadores dessa tabela poderão ser utilizados para que
seja realizada a titulação de uma solução de amônia com
ácido clorídico?
Observe a reação a seguir.
H2C2O4(aq) + 2OH- (aq) → C2O4- (aq) + 2H2O(I)
Suponha que um técnico em química dissolva em água uma
amostra de 1,0g de ácido oxálico impuro e adicione algumas
gotas de indicador ácido-base. Em seguida, ele titula a
solução com NaOH 0,5M. A amostra consome 40mL da solução de
NaOH até atingir o ponto de equivalência. Qual é a massa de
ácido oxálico na amostra inicial?
Assinale a opção que completa corretamente as lacunas da sentença abaixo.
Considere que determinado ácido sofre uma diluição, de modo que sua concentração de íons H+ é alterada de 4x10-7mol/l para 5x10-8 mol/l. Sendo assim, é correto afirmar que o pH da solução original foi alterado de____________ para ___________ .
Dados:
log(2) = 0,301
log(3) = 0,477
log(5) = 0,698