Questões Militares
Sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 116 questões
Bebidas especialmente ingeridas por esportistas têm representado importante fatia de consumo. Tais bebidas são soluções isotônicas repositoras hidroeletrolíticas e, portanto, auxiliam na manutenção e preparação física de atletas de todas as modalidades. A seguir, reproduz-se parte da tabela nutricional constante no rótulo de uma dessas bebidas.

A partir dessas informações e considerando os múltiplos aspectos que
elas suscitam, julgue o item subsequente.
Os cloretos de sódio e de potássio podem ser preparados por
meio da neutralização total do ácido clórico com hidróxidos de
sódio e de potássio, respectivamente.
O óxido de cálcio (CaO) é um óxido ácido.
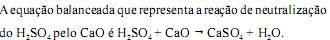
Assinale a opção que apresenta, respectivamente, o tipo de ligações que são encontradas na molécula representada pela fórmula N204 e o nome deste composto.
Um antiácido estomacal contém bicarbonato de sódio (NaHCO3) que neutraliza o excesso de ácido clorídrico (HCl), no suco gástrico, aliviando os sintomas da azia, segundo a equação:
HCl(aq) + NaHCO3(aq) → NaCl(aq) + H2O(l) + CO2(g)
Sobre essas substâncias, são feitas as seguintes afirmações:
I-A fórmula estrutural do bicarbonato de sódio e do ácido clorídrico são respectivamente:
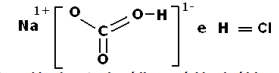
II-Na reação entre o bicarbonato de sódio e o ácido clorídrico, ocorre uma reação de oxidorredução.
III-O antiácido contém 4,200 g de bicarbonato de sódio para neutralização total de 1,825 g do ácido clorídrico presente no suco gástrico.
Dados:
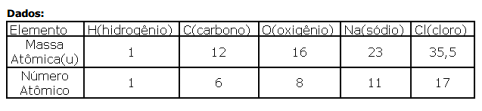
Das afirmações feitas, está(ão) correta(s)
A composição química do cimento Portland, utilizado na construção civil, varia ligeiramente conforme o que está indicado na tabela abaixo:
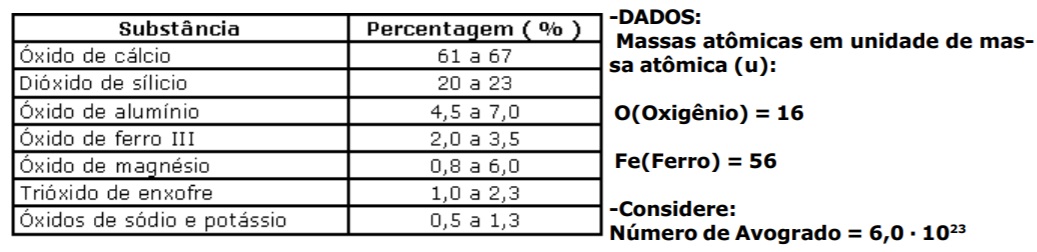
Assinale a alternativa correta:
Considerando que, na titulação do ácido sulfúrico formado no borbulhador, foram gastos 3,2 mol de NaOH e que o totalizador de volume indicou 4 m3 de amostra de ar, conclui-se que, nessa análise, a concentração de dióxido de enxofre no ar amostrado era de 8 × 10-4 mol / L.
O bicarbonato de sódio é um hidrogenossal que apresenta, em sua estrutura, ligações iônicas e covalentes.
Um professor de Química, durante uma aula experimental, pediu a um de seus alunos que fosse até o armário e retornasse trazendo, um por um, nesta ordem: um oxiácido inorgânico; um diácido; um sal de metal alcalino; uma substância que, após aquecimento, pode gerar dióxido de carbono (CO2(g)); e um sal ácido.
Assinale a alternativa que corresponde à sequência de fórmulas moleculares que atenderia corretamente ao pedido do professor.
Uma quantidade de 5828 g de mistura de óxido de sódio(Na2O) e óxido de potássio(K2O) foi tratada com uma solução de ácido clorídrico que continha 300 mols de HCl. Admitindo-se que toda a mistura de óxidos reagiu com parte do HCl, e que o excesso de HCl necessitou de 144 mols de hidróxido de sódio(NaOH) para ser totalmente neutralizado, então a composição percentual, em massa de Na2O e de K2O era, respectivamente,

I - 1 mol de hidróxido de NaOH neutraliza totalmente 1 mol de HCl. II - Trata-se de uma reação de uma base forte com um ácido forte. III - O ácido clorídrico ficará quase que completamente dissociado.
Entre as alternativas certas, encontra (m)-se


