Questões Militares
Sobre técnicas de laboratório em química
Foram encontradas 77 questões
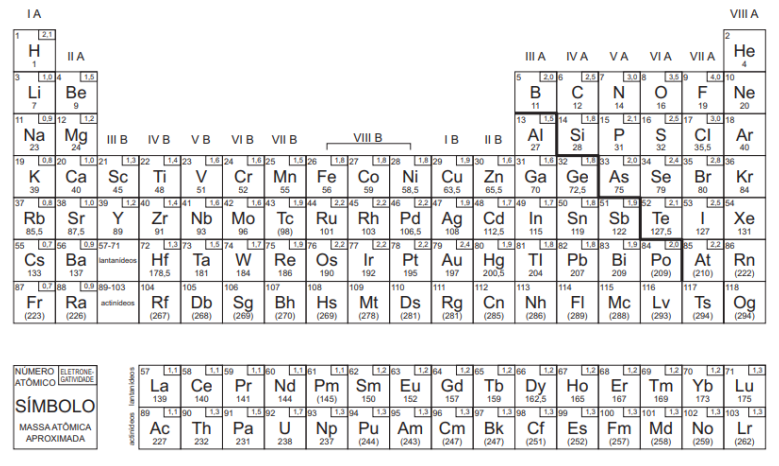
A partir dessas informações, avalie se as afirmativas a seguir são falsas (F) ou verdadeiras (V).
( ) Os elementos apresentados são isótopos entre si.
( ) Ga-68 é o que possui maior número de nêutrons.
( ) F-18 é o que apresenta menor número de massa.
As afirmativas são, respectivamente,

Uma amostra de 2 mL da água de um rio foi misturada com 8 mL de água pura (destilada) de modo a produzir 10 mL de solução. Essa solução foi submetida ao teste com azul de molibdênio que forneceu o resultado de intensidade de cor igual a 3 unidades arbitrárias. O valor de concentração de fosfato na água desse rio é mais próximo de:
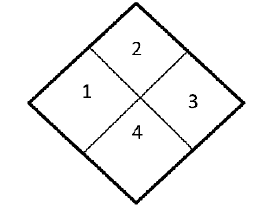
De acordo com o diagrama, a relação entre a cor e o que ela representa na classificação de riscos de produtos químicos está corretamente indicada em
Sobre os tipos de classes, é correto afirmar que
Uma mistura de carbonato de sódio decahidratado e bicarbonato de sódio foi colocada em um cadinho e levada a uma mufla a 350 °C por 3 h, tendo ocorrido as seguintes reações.
Na2CO3 · 10 H2O(s) → Na2CO3(s) + 10 H2O(v)
2 NaHCO3(s) → Na2CO3(s) + H2O(v) + CO2(g)
Finalizado o processo, restou unicamente carbonato de
sódio no cadinho, verificando-se uma perda total de massa de
6,70 g.
Sabendo que M(H) = 1 g/mol, M(C) = 12 g/mol,
M(O) = 16 g/mol e M(Na) = 23 g/mol, e supondo que a
quantidade de CO2 seco desprendido do cadinho seja igual a
2,20 g, assinale a opção que indica a quantidade, em gramas, de
Na2CO3 · 10 H2O existente na mistura inicial.
Constantes
Constante de Avogadro (NA) = 6,02 × 1023 mol−1
Constante de Faraday (F) = 9,65 × 104 C⋅mol−1 = 9,65 × 104 A⋅s⋅mol−1 = 9,65 × 104 J⋅V−1 ⋅mol−1
Carga elementar = 1,60 × 10−19 C
Constante dos gases (R) = 8,21 × 10−2 atm⋅L⋅K−1⋅mol−1 = 8,31 J⋅K −1 ⋅mol−1 = 1,98 cal⋅K−1 ⋅mol−1
Constante de Planck (h) = 6,63 × 10−34 J⋅s
Velocidade da luz no vácuo = 3,0 × 108 m⋅s −1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 × 105 N⋅m−2 = 1,01325 bar
Energia: 1 J = 1 N⋅m = 1 kg⋅m2 ⋅s−2 = 6,24 × 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 °C e 1 atm
Condições ambientes: 25 °C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol⋅L−1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol⋅L−1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio

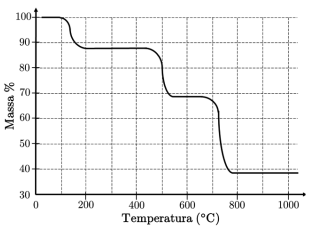
Com base nessa figura e sabendo que a massa inicial corresponde a 100%, é ERRADO afirmar que
Constantes
Constante de Avogadro (NA) = 6,02 × 1023 mol−1
Constante de Faraday (F) = 9,65 × 104 C⋅mol−1 = 9,65 × 104 A⋅s⋅mol−1 = 9,65 × 104 J⋅V−1 ⋅mol−1
Carga elementar = 1,60 × 10−19 C
Constante dos gases (R) = 8,21 × 10−2 atm⋅L⋅K−1⋅mol−1 = 8,31 J⋅K −1 ⋅mol−1 = 1,98 cal⋅K−1 ⋅mol−1
Constante de Planck (h) = 6,63 × 10−34 J⋅s
Velocidade da luz no vácuo = 3,0 × 108 m⋅s −1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 × 105 N⋅m−2 = 1,01325 bar
Energia: 1 J = 1 N⋅m = 1 kg⋅m2 ⋅s−2 = 6,24 × 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 °C e 1 atm
Condições ambientes: 25 °C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol⋅L−1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol⋅L−1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio

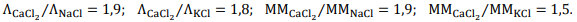
Com base nessas informações, assinale a opção CORRETA entre as condutividades das soluções.
A decomposição térmica do oxalato de cálcio anidro inicia em cerca de 400 ºC e ocorre em duas etapas representadas pelas equações. O composto sólido formado na primeira reação se decompõe em cerca de 600 o C.
CaC2O4 (s) → CaCO3 (s) + CO (g) CaCO3 (s) → CaO (s) + CO2 (g)
O resultado da análise é apresentado na forma de uma curva da variação de massa em função da temperatura ao longo do processo de aquecimento.
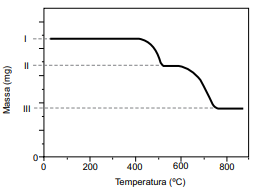
(Cavalheir, E. T. G.; et al. Química Nova. Adaptado)
I. 51,2 mg da amostra da mistura de CaC2O4 e SiO2. II. 42,8 mg. III. 29,6 mg.
O teor de oxalato de cálcio nessa amostra é de
Água potável não é adequada para o preparo de soluções em laboratórios clínicos. Nesse caso, recomenda-se o uso de água tratada pelos processos de destilação, deionização, osmose reversa ou filtração.
De maneira geral, ao se preparar soluções salinas, o ajuste para o volume final deve ser feito em um béquer, em virtude de sua maior exatidão.
Coloque F (falso) ou V (verdadeiro) nas afirmativas abaixo, em relação às técnicas básicas para análises em laboratório, assinalando a seguir a opção correta.
( ) As laterais da câmara de pesagem da balança analítica de prato único não precisam ser fechadas, tendo em vista que a medição nesse tipo de equipamento não é afetada por correntes de ar externo.
( ) A calcinação de precipitados é feita em cadinhos de porcelana, em atmosfera oxidante e de maneira bem lenta, de forma que não haja nenhuma mudança química do precipitado causada pelo carbono proveniente da queima do papel-filtro.
( ) A calibração é o processo para medir a quantidade real de uma grandeza que corresponde à quantidade indicada na escala de um instrumento.
( ) Durante o processo de limpeza, um aparelho volumétrico deve ser aquecido para remoção de gorduras e impurezas porventura contidas nas suas paredes internas, haja vista que esses equipamentos não deformam durante o procedimento.
( ) A água-régia, substância empregada no preparo de soluções em gravimetria, é utilizada para a solubilização de metais.
O tratamento quantitativo da absorção de energia radiante pela matéria depende do princípio geral conhecido como Lei de Beer, a qual se encontra abaixo representada:
A = a.b.c, onde
A = Absorbância, a = absortividade, b = caminho óptico da amostra, c = concentração do absorvente.
Em relação à Lei de Beer e seus parâmetros, é correto afirmar que: