Questões Militares de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
Foram encontradas 102 questões
Observe as reações químicas a seguir.
H2O(I) → H2(g) + 1/2O2(g) Δh = +283 kJ
H2(g) + 1/2O2(g) → H2O(g) Δh = -242 kJ
Qual é o valor do calor de vaporização da água?
Sabendo que a energia de ligação entre dois átomos representa a energia que seria necessária para separá-los a uma distância de separação infinita, observe a tabela a seguir com os valores de energia de ligação para algumas substâncias.
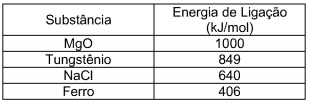
A partir da análise simples dos dados da tabela acima, foram tiradas as seguintes conclusões; analise-as.
I. A temperatura de fusão do tungstênio é maior que a do ferro.
II. A temperatura de fusão do MgO é maior que a do tungstênio.
III. A temperatura de fusão do NaCI é maior que a do ferro.
IV. A temperatura de fusão do MgO é maior que a do NaCI.
As conclusões corretas, que podem ser tiradas a partir da análise simples dos dados dessa tabela, são apenas
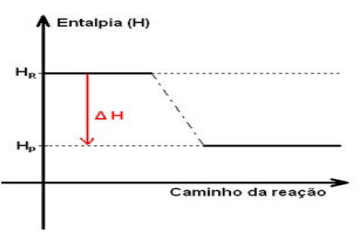
De acordo com o gráfico acima pode concluir se que trata se de uma reação Hp = 250, Hr = 480: I - Espontânea. II - Exotérmica, pois ocorreu um ganho de energia. III - Necessita apenas de um estímulo para que ocorra. IV - Sendo o Hp = 250 kj e Hr = 480kj o delta será de +130 kj. V - Endotérmica, pois ocorreu uma perda de energia. VI - Sendo o Hp = 250 e Hr = 480 delta H será de -130kj. Estão incorretas:
Considere duas reações químicas, mantidas à temperatura e pressão ambientes, descritas pelas equações abaixo:
I. H2(g) + 1/2 O2(g) → H2O(g)
ΙΙ. H2(g) + 1/2O2(g) → H2O(l )
Assinale a opção que apresenta a afirmação ERRADA sobre estas reações.
Sabe-se que a 25 °C as entalpias de combustão (em kJ mol−1) de grafita, gás hidrogênio e gás metano são, respectivamente: –393,5; –285,9 e –890,5. Assinale a alternativa que apresenta o valor CORRETO da entalpia da seguinte reação:
C(grafita) + 2H2 (g) → CH4(g)
