Questões Militares
Comentadas sobre transformações químicas e energia em química
Foram encontradas 267 questões
( ) No meio não aerado, o hidrogênio pode ficar adsorvido na superfície do catodo, polarizando a pilha formada com conseqüente redução do processo corrosivo.
( ) Se o oxigênio puder ser rápido e uniformemente fornecido a uma superfície metálica, é possível reparar fraturas que ocorram na película, diminuindo-se, assim, a velocidade de corrosão.
( ) O cobre tem uma velocidade de corrosão rápida em presença de ácidos não oxidantes, e em presença de oxigênio este vai funcionar como estimulador de corrosão.
( ) A corrosão eletroquímica será tanto mais intensa quanto maior o valor do pH.
( ) O cobre se mostra eficaz quando disperso em resina, geralmente epóxi, ou em silicatos inorgânicos ou orgânicos.
( ) No mecanismo de barreira, a eficiência da proteção depende da espessura do revestimento e da resistência das tintas ao meio corrosivo.
( ) No mecanismo de inibição, as tintas de fundo contêm determinados pigmentos inibidores que dão origem à formação de uma camada passiva sobre a superfície do metal, impedindo a sua passagem para a forma iônica.
Diferentes marcas de telefones celulares buscam ganhar novos clientes, anunciando que a bateria de seus aparelhos é mais eficiente que a dos concorrentes, por manterem o telefone celular ligado por mais tempo. Quando descarregada, a bateria do celular é conectada a uma rede elétrica para que sua carga seja restabelecida.
Esse processo é um exemplo de:
Observe as reações químicas a seguir.
H2O(I) → H2(g) + 1/2O2(g) Δh = +283 kJ
H2(g) + 1/2O2(g) → H2O(g) Δh = -242 kJ
Qual é o valor do calor de vaporização da água?
Observe a reação de oxirredução não balanceada a seguir.
Cu(s) + Ag+(aq) → Ag(s) + Cu2+(aq)
A soma de todos os coeficientes estequiométricos da reação
balanceada é :
Sabendo-se que
( 1 ) Mg → Mg2+ + 2e- com E10 = 2,37 V, e
( 2 ) Sn2+ + 2e- → Sn com E20 = -0,14 V,
Em que E10 e E20 são as tensões elétricas decorrentes dessas reações, respectivamente, calcule a tensão obtida na reação abaixo.
Mg(s) + Sn2+ → Mg2+ + Sn
Sendo assim, assinale a opção correta.
I. X(g)+e–→ X (g)+E1 II. X (g)+E2→X(g)+e- III. X(g)+E3→ X+(g)+e- IV. X+ (g)+E4→X2+ (g)+e-
Com base nas equações representadas, pode-se afirmar que:
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2Pb2+ SO4 2- (aq) + 2H2O(ℓ)
São feitas as seguintes comparações sobre as capacidades caloríficas de diferentes substâncias puras, todas à temperatura ambiente:
I. A capacidade calorífica da água é menor que a do peróxido de hidrogênio.
II. A capacidade calorífica do bromo é menor que a do tetracloreto de carbono.
III. A capacidade calorífica do metanol é menor que a do mercúrio.
Assinale a opção que apresenta(s) comparação(ões) CORRETA(S).
É de 0,76 V a força eletromotriz padrão, E°, de uma célula eletroquímica, conforme a reação
Zn(s) + 2H+ (aq) → Zn2+ (aq) + H2 (g).
A análise dos dados termodinâmicos de reações permite a previsão da espontaneidade. Na tabela a seguir estão apresentados os dados termodinâmicos de duas reações químicas.
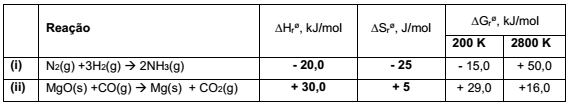
A partir dos dados apresentados, identifique as seguintes afirmativas como verdadeiras (V) ou falsas (F):
( ) A diminuição da temperatura desfavorece a espontaneidade da reação (i).
( ) O aumento da temperatura favorece a espontaneidade da reação (ii).
( ) Na temperatura de 400 K, a reação (i) será espontânea.
( ) Na temperatura de 4000 K, a reação (ii) será espontânea.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.