Questões Militares de Química - Transformações Químicas e Energia
Foram encontradas 372 questões
Coloque V (verdadeiro) ou F (falso) nas afirmativas abaixo, com relação à corrosão de metais, assinalando a seguir a opção correta.
( ) A passivação de um metal pode ser obtida por meio da oxidação ou por polarização anódica.
( ) Uma das formas de atenuar a corrosão galvânica em estruturas compostas de materiais metálicos diferentes é utilizar o metal catódico para confecção das peças pequenas e, para as peças maiores da estrutura, metal anódico .
( ) A corrosão eletrolítica pode ser diminuída se o valor da corrente elétrica de interferência for aumentado.
( ) Na zona de respingos, próxima à faixa de variação das marés, a ação corrosiva é mais acentuada devido a diversos fatores, dentre eles a salinidade da água do mar e a ação mecânica das ondas.
Analise a tabela abaixo .

Com relação aos dados contidos na tabela acima, assinale a
opção correta.
Um isótopo radioativo de Urânio-238 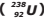 , de número atômico 92 e número de massa 238,
emite uma partícula alfa, transformando-se num átomo X, o qual emite uma partícula beta, produzindo
um átomo Z, que por sua vez emite uma partícula beta, transformando-se num átomo M. Um
estudante analisando essas situações faz as seguintes observações:
, de número atômico 92 e número de massa 238,
emite uma partícula alfa, transformando-se num átomo X, o qual emite uma partícula beta, produzindo
um átomo Z, que por sua vez emite uma partícula beta, transformando-se num átomo M. Um
estudante analisando essas situações faz as seguintes observações:
I – os átomos X e Z são isóbaros;
II – o átomo M é isótopo do Urânio-238 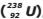
III – o átomo Z possui 143 nêutrons;
IV – o átomo X possui 90 prótons.
Das observações feitas, utilizando os dados acima, estão corretas:

II – a reação Zn2+(aq) + Cu º(s) ➞ Zn º(s) + Cu2+(aq) não é espontânea;
III – pode-se estocar, por tempo indeterminado, uma solução de nitrato de níquel II, em um recipiente revestido de zinco, sem danificá-lo, pois não haverá reação entre a solução estocada e o revestimento de zinco do recipiente;
IV – a força eletromotriz de uma pilha eletroquímica formada por chumbo e magnésio é 2,24 V;
V – uma pilha eletroquímica montada com eletrodos de cobre e prata possui a equação global: 2 Ag+ (aq) + Cuº(s) ➞ 2 Agº(s) + Cu2+ (aq) .
DADOS:
Constante de Faraday= 96500 Coulombs/mol de elétrons
Massa molar do níquel=59 g/mol
Massa molar da prata=108 g/mol

Esse conjunto de cubas em série é ligado a uma bateria
durante um certo intervalo de tempo, sendo observado
um incremento de 54 g de massa de prata em um dos
eletrodos de prata. Desse modo, o incremento da massa
de níquel em um dos eletrodos de níquel é de