Questões Militares de Química - Transformações Químicas e Energia
Foram encontradas 372 questões
Substância Massa específica (g ∙ cm−3) Calor específico (J ∙ g−1 ∙ K−1)
H2O 1,00 4,18
Ti 4,54 0,52
Cr 7,18 0,45
Ni 8,90 0,44
Em um experimento de laboratório, cloreto de alumínio, cloreto de zinco e carbonato de sódio são dissolvidos, individualmente, em três recipientes separados contendo água neutra aerada com pH = 7. Uma placa de ferro metálico é imersa em cada um dos recipientes, que são mantidos à temperatura de 25 °C.
Admitindo-se as condições experimentais apresentadas acima, são feitas as seguintes afirmações em relação à influência da hidrólise dos sais na velocidade de corrosão das placas metálicas:
I. O cátion alumínio hidratado forma soluções aquosas que aceleram a corrosão do ferro.
II. As soluções aquosas produzidas pela hidrólise do ânion carbonato inibem a corrosão do ferro.
III. A corrosão do ferro é inibida pela solução aquosa formada no processo de hidrólise do cátion zinco hidratado.
Das afirmações acima, está(ão) CORRETA(S) apenas
Assinale a opção CORRETA que apresenta o potencial de equilíbrio do eletrodo A l3+ /A l ,em volt, na escala do eletrodo de referência de cobre-sulfato de cobre, à temperatura de 25 °C, calculado para uma concentração do íon alumínio de 10-3 mol-1 .
Dados: Potenciais de eletrodo padrão do cobre-sulfato de cobre
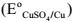 e do alumínio
e do alumínio 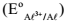 , na escala do
eletrodo de hidrogênio, nas condições-padrão:
, na escala do
eletrodo de hidrogênio, nas condições-padrão: 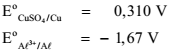
Em um experimento eletrolítico, uma corrente elétrica circula através de duas células durante 5 horas. Cada célula contém condutores eletrônicos de platina. A primeira célula contém solução aquosa de íons Au3+ enquanto que, na segunda célula, está presente uma solução aquosa de íons Cu2+ .
Sabendo que 9,85 g de ouro puro foram depositados na primeira célula, assinale a opção que corresponde à massa de cobre, em gramas, depositada na segunda célula eletrolítica.
Considere a energia liberada em
I. combustão completa (estequiométrica) do octano e em
II. célula de combustível de hidrogênio e oxigênio.
Assinale a opção que apresenta a razão CORRETA entre a quantidade de energia liberada por átomo de hidrogênio na combustão do octano e na célula de combustível.
Dados: Energias de ligação, em KJ mol-1:
C – C 347 H – H 436
C – H 413 H – O 464
C = O 803 O = O 498