Questões de Concurso Militar EsFCEx 2014 para Oficial - Magistério Química
Foram encontradas 70 questões
Marque a opção correta.
Para a reação representada abaixo, a constante de equilíbrio, Keq, é descrita como:

São dadas as energias de ligação H - X, para X = F, Cℓ, Br, I
HF(g) 567 kJ/mol
HCℓ(g) 431 kJ/mol
HBr(g) 366 kJ/mol
HI(g) 299 kJ/mol
I. H2PO4 (aq) + H2O(ℓ) → HPO4 2 (aq) + H3O (aq) II. HPO4 2 (aq) + H2O(ℓ) → H2PO4 (aq) + OH (aq) III. [Aℓ(H2O)6]3 (aq) + H2O(ℓ) → [Aℓ(H2O)5OH]2 (aq) + H3O (aq) IV. CaO(s) + H2O(ℓ) → Ca2 (aq) + 2 OH (aq)
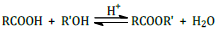
Essa reação é classificada como:
I. O nome IUPAC é propanoato de etila. II. O ácido carboxílico que dá origem a esse éster é o propanóico. III. A hidrólise básica deste éster forma o ânion etanoato. IV. O álcool necessário para obter esse éster é o propan-1-ol.
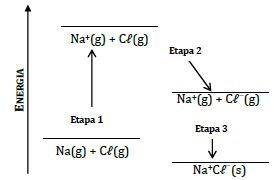
As energias envolvidas nas etapas 1, 2 e 3 são denominadas, respectivamente:
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2Pb2+ SO4 2- (aq) + 2H2O(ℓ)
I. As proporções molares com que os produtos são formados. II. Que a reação pode ocorrer. III. Que a reação é exotérmica. IV. A espontaneidade da reação. V. As fórmulas dos produtos.
I. X(g)+e–→ X (g)+E1 II. X (g)+E2→X(g)+e- III. X(g)+E3→ X+(g)+e- IV. X+ (g)+E4→X2+ (g)+e-
Com base nas equações representadas, pode-se afirmar que:

I. Em uma solução de NaCℓ em água há interações íon-dipolo. II. Em uma solução de oxigênio (O2) em água há interações dipolo - dipolo induzido. III. Em uma solução de iodo (I2) em tetracloreto de carbono (CCℓ4) há interações dipolo instantâneo-dipolo induzido.
C3H5(ONO2)3(ℓ)→N2(g)+CO2(g)+O2(g)+H2O(g)
Qual o volume aproximado de gás formado, ao nível do mar e a 27ºC, quando 2,27g da dinamite reagem?
Marque a alternativa correta.
A variação de entropia mede o grau de desordem em um processo. A seguir são apresentados alguns processos físicos ou químicos.
I. H2O(ℓ) → H2O(g)
II. H2O(ℓ) a 20 oC → H2O(ℓ) a 80 oC
III. NaCℓ(s) + H2O(ℓ) → Na+(aq) + Cℓ(aq)
IV. 2NH3(g) N2(g) + 3H2(g)
As equações que representam aumento de entropia são: