Questões de Concurso Militar CAP 2017 para Cabo - Técnico em Química
Foram encontradas 9 questões
Calcule o potencial da célula Zn|ZnSO4||CuSO4|Cu e indique se a reação Zn(s)+ Cu2+ -> Zn2+ + Cu(s) ocorre de forma espontânea ou não, marcando a opção correta.
Dados: E0Cu = +0,337V; E0Zn = -0.763V
Analise os potenciais padrão dos eletrodos de prata e zinco abaixo.
Ag+ + e- ↔ Ag E° = + 0,7999 V
Zn2+ + 2e- ↔ Zn E° = - 0,763 V
Assinale a opção que apresenta a reação da pilha dos
potenciais padrão acima.
Calcule a f.e.m. de uma célula formada pela imersão de uma lâmina de cobre numa solução de 0,15M de CuSO4 e um bastão de zinco numa solução de 0,25M de ZnSO4 e marque a opção correta.
Dados:
Equação de Nernst: E = E0 + (0,0592/n) x log M
Cu2+ + 2e- = Cu; E0Cu = 0,34V
Zn2+ + 2e- = Zn; E0Zn = -0,76V
log(0,15) = -0,82391
log(0,25) = -0,60206
Considere as seguintes equações termoquímicas:
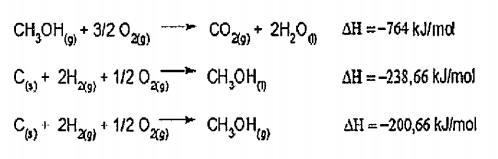
A entalpia de combustão para o metanol líquido, em
kJ/mol, é:
O etanoi é um combustível obtido a partir de fontes renováveis, e cuja equação de combustão a 25°C é a seguinte:
C2H5OH(I) + 3O2(g) → 2CO2(g) + 3H2O(I) ΔH298 =-1368 kJ/mol
Sabendo-se que um volume de 8,05 litros de etanol foi queimado, a quantidade total de calor liberado, em kJ, na combustão acima é:
Dado: densidade do etanoi = 0,8 g/cm3