Questões Militares Comentadas por alunos sobre transformações gasosas em física
Foram encontradas 52 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A uma pressão P e temperatura T, n moles de gás ideal
realizam uma expansão isotérmica reversível passando de um volume inicial V1 para um volume final 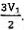 Se 2n moles do mesmo gás, a uma pressão P e temperatura T/4 realizam outra expansão isotérmica, passando de um
volume inicial Vi a um volume final Vf , e o trabalho
realizado nas duas transformações foi o mesmo, então o quociente
Se 2n moles do mesmo gás, a uma pressão P e temperatura T/4 realizam outra expansão isotérmica, passando de um
volume inicial Vi a um volume final Vf , e o trabalho
realizado nas duas transformações foi o mesmo, então o quociente 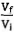 é igual a
é igual a
Analise as afirmativas a seguir.
I. Em uma expansão isotérmica reversível, o sistema recebe uma quantidade de calor da fonte de aquecimento.
II. Em uma expansão adiabática reversível, o sistema não troca calor com as fontes térmicas (M-N).
III. Em uma compressão isotérmica reversível, o sistema não cede calor para a fonte de resfriamento.
IV. Em uma compressão adiabática reversível, o sistema não troca calor com as fontes térmicas.
V. Numa máquina de Carnot, a quantidade de calor que é fornecida pela fonte de aquecimento e a quantidade cedida à fonte de resfriamento são proporcionais às suas temperaturas absolutas.
Estão corretas apenas as afirmativas.
Analise as figuras a seguir.
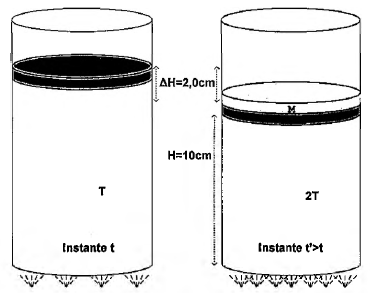
As figuras acima mostram dois instantes diferentes, t e t' de um mesmo sistema, imerso no ar ao nível do mar. O sistema é constituído por um cilindro, cuja área da base é de 3,0cm2, contendo um gás ideal comprimido por um pistão móvel de massa desprezível. No instante t, a base do cilindro está em contato com uma chama que mantém o gás a uma temperatura T. No instante t', a base do cilindro está em contato com uma chama mais intensa que mantém o gás a uma temperatura 2T, e sobre o pistão encontra-se uma massa M que promove um deslocamento do pistão de 2,0cm para baixo. Qual o valor da massa M, em kg?
Dados: g = 10 m/s2
po = 105Pa
Observe o diagrama pressão versus volume a seguir.
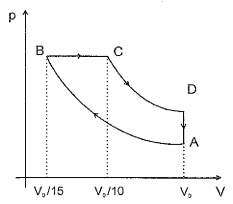
Esse diagrama representa uma máquina térmica operando o chamado Ciclo de Diesel, era que 10 moles de uma mistura de ar e gasolina (tratada como um gás ideal) sofrem uma compressão adiabática (AB), depois um aquecimento à pressão constante (BC), seguido por uma expansão adiabática (CD), que move o pistão, e, finalmente, um resfriamento isométrico (DA), retornando ao estado inicial. Como o ar é essencialmente uma mistura de gases diatômicos, considere a capacidade térmica à pressão constante do gás em questão como Cp= (7/2) R.
Considerando ainda o ponto A nas CNTP e sabendo que a pressão no trecho BC é 55atm, calcule o calor absorvido neste trecho e assinale a opção correta.
Dado: R=8,31 J/molKAnalise o diagrama abaixo.
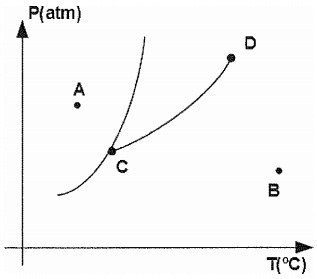
Considerando o diagrama de fases de uma substância simples representado na figura acima, analise as afirmativas abaixo.
I - Partindo do estado A, não é possível fundir a substância em uma expansão isotérmica.
II - A curva CD define todos os pontos de pressão máxima de vapor.
III- Se a substância for comprimida isotermicamente a partir do estado B poderá ocorrer liquefação.
IV - Se, a partir do estado A, a pressão for mantida constante e a temperatura aumentar, a substância poderá sofrer duas mudanças de fase.
Assinale a opção correta.