Questões Militares
Foram encontradas 105 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere a reação reversível à seguir.
A + B <-> C + D
Sabendo-se que a notação [x] indica a concentração de um
determinado componente x, assinale a opção que apresenta o
valor da constante de equilíbrio da reação.
Com relação ao equilíbrio das reações químicas, analise as afirmativas abaixo.
I - A expressão matemática da constante de equilíbrio (K) relaciona as concentrações de reagentes e produtos no equilíbrio.
II - Os efeitos da perturbação de um equilíbrio químico são previstos pelo Princípio de Le Chatelier.
III- Quando o valor da constante de equilíbrio for grande (K muito maior que 1), a reação é favorável aos reagentes e as concentrações dos produtos no equilíbrio são menores que as dos reagentes.
Assinale a opção correta.
Uma barra de ferro e um fio de platina, conectados eletricamente a um voltímetro de alta
impedância, são parcialmente imersos em uma mistura de soluções aquosas de FeSO4 (1,0 mol L–1) e HCl isenta de oxigênio. Um fluxo de gás hidrogênio é mantido constante sobre a parte imersa da superfície da
platina, com pressão nominal (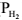 ) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
Considerando-se que ambos os metais são quimicamente puros e que a platina é o polo positivo do elemento galvânico formado, assinale a opção CORRETA que apresenta o valor calculado do pH desse meio aquoso.
Dados: 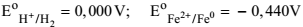
Um erlenmeyer contém 10,0 mL de uma solução de ácido clorídrico, juntamente com algumas gotas de uma solução de fenolftaleína. De uma bureta, foi-se gotejando uma solução 0,100 M de hidróxido de sódio até o aparecimento de leve coloração rósea. Nesse momento, observou-se um consumo de 20,0 mL da solução alcalina. Pode-se afirmar que a concentração de HCl na solução ácida original era de:
Dados:
Massas atômicas: H = 1,00 u, O = 16,0 u, Na = 23,0 u, Cl = 35,5 u
