Questões Militares
Para magistério superior
Foram encontradas 333 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Café, chocolate e chá tornaram-se bebidas muito apreciadas quando__________ o açúcar. Já as frutas, alguns estudiosos____________ , até então, apenas um remédio; porém, associadas ao açúcar, passaram a saborosas sobremesas.
De acordo com a colocação dos pronomes e com o emprego do sinal indicativo de crase determinados pela norma-padrão, as lacunas desse texto devem ser preenchidas, respectivamente, por:
Considere a reação química de formação de uma molécula de triglicerídeo.
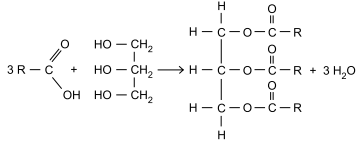
Sobre os reagentes e produtos, assinale a alternativa
correta.
Analise a biomolécula.
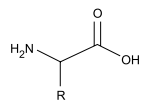
A biomolécula ilustrada é de um
O processo de obtenção sustentável do monômero é corretamente representado em:

Assinale a alternativa que completa, correta e respectivamente, as lacunas.
Substância Constante HCl Muito grande NaOH Grande CH3COOH 1,8 x 10–5 NH4OH 1,8 x 10–5 H2CO3 K1 : 4,2 x 10–7 K2 : 4,8 x 10–11
Analise o diagrama.
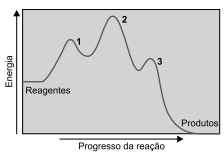
O diagrama representa uma reação _________, que ocorre em três etapas, sendo a mais _________ a etapa 3, porque possui _________ energia de ativação.
Assinale a alternativa que completa, correta e respectivamente, as lacunas.
T (ºC) Kw 10 0,29 × 10–14 15 0,45 × 10–14 20 0,68 × 10–14 25 1,01 × 10–14 30 1,47 × 10–14 50 5,48 × 10–14
Os valores de Kw mostram que, a 50 ºC, o pH da água pura é
2 SO2 (g) + O2(g) ⇌ 2 SO3(g) Temperatura, K Constante, Kc 300 4 x 1024 500 2,5 x 1010 700 3,0 x 104
As melhores condições para que a formação do produto seja favorecida são:
Considerando a constante de Faraday 9,65 x 104 C.mol–1, a massa máxima de níquel e ouro depositadas nesse período de funcionamento do sistema foi, respectivamente, de, aproximadamente,
2 Na+(eletrólito) + 2 e– → 2 Na(l) Eº = –2,71 V S8 (l) + 16 e– → 8 S2– (eletrólito) Eº = –0,51 V
O potencial padrão dessa bateria e o número de elétrons transferidos para cada molécula S8(l), são, respectivamente,
I. NH4+ + NH2– → 2NH3. II. CH3NH2 + H2O → CH3NH3+ + OH– III. SO3 2– + S → S2O3 2–
As espécies que atuam como ácido nas reações representadas em I, II e III são, respectivamente,
A decomposição térmica do oxalato de cálcio anidro inicia em cerca de 400 ºC e ocorre em duas etapas representadas pelas equações. O composto sólido formado na primeira reação se decompõe em cerca de 600 o C.
CaC2O4 (s) → CaCO3 (s) + CO (g) CaCO3 (s) → CaO (s) + CO2 (g)
O resultado da análise é apresentado na forma de uma curva da variação de massa em função da temperatura ao longo do processo de aquecimento.
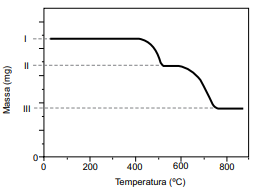
(Cavalheir, E. T. G.; et al. Química Nova. Adaptado)
I. 51,2 mg da amostra da mistura de CaC2O4 e SiO2. II. 42,8 mg. III. 29,6 mg.
O teor de oxalato de cálcio nessa amostra é de
Considerando que a reação cessa após o consumo total do reagente limitante, ao serem misturados 12 mol de cada um dos reagentes, a quantidade máxima de fosfeto de boro que pode ser formada e a quantidade total de reagentes que permanecem sem reagir são, respectivamente,
Considere a curva de solubilidade da sacarose.
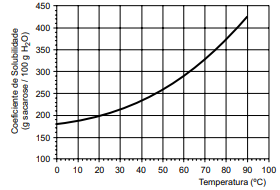
A temperatura em que se iniciou a cristalização e a massa máxima de açúcar cristalizada na solução em repouso a 20 ºC são, correta e respectivamente,
Considerando que se empregou a técnica quantitativa na preparação da solução, a concentração de íons nitrato na solução preparada é