Questões de Concurso
Comentadas sobre equilíbrio químico em química
Foram encontradas 606 questões
HCI (aq) + KOH (aq) → KCI (aq) + H2O (I)
Após os cálculos, esse pós-graduando concluiu que o pH da solução resultante é igual a:
Dados: αHCl = 100%, Log 5 = 0,7 Massas Molares em g/mol: H = 1; O = 16; Cl = 35,5; K=39,1
Considere a mistura de 100 mL de sulfeto de sódio 0,2 mol L−1 com 100 mL de nitrato de chumbo 0,1 mol L−1 , resultando na formação do precipitado sulfeto de chumbo. A solubilidade, em mol L−1 , do sulfeto de chumbo na solução é de
(Dado: Kps PbS = 3,0x10−28)
(Dado: log 8,5 = 0,93)
O íon complexo [Zn(NH3)]+2 é formado a partir 3 4 da seguinte reação química:
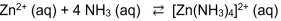
Em um experimento, ao se atingir o equilíbrio químico, as concentrações dos participantes da reação são apresentadas na tabela a seguir.
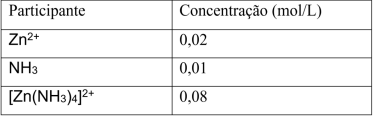
A constante de equilíbrio dessa reação é igual a:

Para melhorar o rendimento dessa síntese, duas modificações podem ser feitas sobre o sistema:
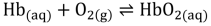
(Onde Hb é a hemoglobina e HbO é oxi- 2 hemoglobina.) O rendimento físico de um atleta está ligado, entre outros fatores, à capacidade de metabolizar oxigênio, o que pode ser prejudicado pela altitude na qual a atividade física está sendo realizada. Assim, um atleta acostumado a treinar no Rio de Janeiro (nível do mar) tem seus resultados físicos prejudicados quando compete na Cidade do México (2250 m acima do nível do mar) pois, nessa altitude, a pressão:
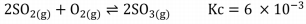
Considerando que a reação foi mantida em um recipiente de 2 L a 300K e as quantidades de dióxido de enxofre e de oxigênio no equilíbrio são 0,2 e 1,2 mols respectivamente, a concentração molar do produto obtido no equilíbrio é de:
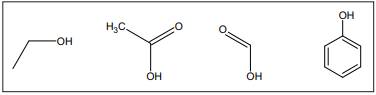
Em uma reação de esterificação, o pKa do catalisador é um fator muito importante para o melhor rendimento do produto de interesse. Dentre os compostos apresentados, a ordem crescente de pKa é:
Fe2O3 (s) + x H+ (aq) ⇌ y Fe3+ (aq) + z H2O (l)
Com base nessas informações, julgue o seguinte item.
A constante de equilíbrio K da reação do óxido de ferro (III) é corretamente expressa pela seguinte equação. K = [ Fe3+ ]y [ H20]z / [Fe2O3] [ H+]x
3 Cuo(s) + 8 HNO3(aq) → 3 Cu(NO3)2(aq) + 2 NO(g) + 4 H2O(l) (1) 2 NO(g) + O2(g) → 2 NO2(g) (2) NO2(g) ⇌ N2O4(g) (3)
Isso posto, considerando um sistema transparente e fechado, o produto NO2(g) apresenta coloração marrom. O produto N2O4(g) é um gás incolor e, quando o sistema é aquecido acima da temperatura ambiente, o sistema apresenta uma coloração marrom (forte). Em relação à equação três, referente à formação do N2O4(g), é correto afirmar que: