Questões de Concurso
Sobre equipamentos e técnicas básicas em química
Foram encontradas 1.471 questões
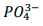 foi precipitado como Ag3PO4 a partir da adição
de 20mL de AgNO3 0,4mol.L-1. O excesso de AgNO3 foi retrotitulado com 5,2 mL de KSCN 0,17 mol.L-1. A
porcentagem aproximada de fósforo na amostra de
fertilizante é
[Ma(u): Ag = 108; K = 39; S = 32; P = 31; O = 16; N= 14; C =
12]:
foi precipitado como Ag3PO4 a partir da adição
de 20mL de AgNO3 0,4mol.L-1. O excesso de AgNO3 foi retrotitulado com 5,2 mL de KSCN 0,17 mol.L-1. A
porcentagem aproximada de fósforo na amostra de
fertilizante é
[Ma(u): Ag = 108; K = 39; S = 32; P = 31; O = 16; N= 14; C =
12]: No que se refere aos métodos gerais de química orgânica e às propriedades e às características dos compostos orgânicos, julgue o item.
A espectrometria de ressonância magnética nuclear dá
informações detalhadas sobre a conectividade atômica
das moléculas, testando os núcleos de uma estrutura e
de seus vizinhos, mas sendo restrita aos átomos de
carbono e de hidrogênio.
Adicionar 50,0 mL de gasolina a uma proveta de 100 mL com tampa esmerilhada; Adicionar, na mesma proveta, 50,0 mL da solução de cloreto de sódio 10% (massa/volume), recém preparada; Tampar a proveta e inverter 10 vezes a proveta e aguardar 10 minutos para realizar a leitura; Após os 10 minutos (tempo para a nítida separação entre as fases), registrar o volume da fase aquosa. O volume da fase aquosa, inicialmente 50,0 mL, sofre um aumento após a mistura com a fase orgânica.
Resultado: Após três determinações, o volume da fase aquosa aumentou de 50,0 mL para 64,0 mL, nas três determinações.
A porcentagem encontrada de etanol na gasolina foi:
1- Difração de raios X de pó
( ) Investigação de propriedades de materiais que podem ser aplicados em telas de dispositivos eletrônicos.
2- Difração de raios X de monocristal
( ) Determinação da estrutura de moléculas e redes estendidas.
3- Espectroscopia no Ultravioletavisível
( ) Determinação de estruturas moleculares em solução e líquidos puros.
4- Espectroscopia de Emissão
( ) Determinação das energias das vibrações moleculares.
5- Espectroscopia no Infravermelho e Raman
( ) Energias e intensidades das transições eletrônicas fornecem informações sobre a estrutura eletrônica e o ambiente químico do ligante sobre o íon ou átomo “d”.
6- Ressonância Magnética Nuclear
( ) Identificação das fases e determinação dos
parâmetros e do tipo de rede.
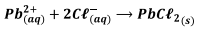
Admite-se que os íons Pb2+ foram consumidos em sua totalidade formando cloreto de chumbo(Il). O excesso de ácido é titulado com solução 0,1 mol.L-1 de hidróxido de sódio (NaOH), consumindo 30mL da base.
O teor (em base mássica) de ions Pb2+ na amostra de efluente, expresso em porcentagem, é aproximadamente iguala:
[Ma(u): Pb = 207; Cl 35,5; Na=23;0=16;H=1]
Um técnico coletou uma alíquota de 200mL dessa última solução e adicionou 600mL de solução aquosa de NaCl 0,5 mol.L-1. A concentração de K2CO3, em mol.L-1, na solução salina preparada pelo técnico corresponde a:
[Ma(u): K = 39; Cl 35,5; Na = 23; 0= 16; C = 12]
[Ma(u): Ba =137;0=16;N=14;H=1]